13.2.2019, Journal of Feline Medicine and Surgery; Preklad 10.2.2021
Pôvodný článok: Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis
Niels C Pedersen, Michel Perron, Michael Bannasch, Elizabeth Montgomery, Eisuke Murakami, Molly Liepnieks, and Hongwei Liu
Abstrakt
Ciele
Cieľom tejto štúdie bolo zistiť bezpečnosť a účinnosť nukleozidového analógu GS-441524 pre mačky trpiace rôznymi formami prirodzene získanej infekčnej peritonitídy mačiek (FIP).
Metódy
Mačky boli vo veku od 3,4 do 73 mesiacov (priemerne 13,6 mesiaca); 26 mačiek malo vlhkú alebo zmiešanú FIP, 5 suchú formu FIP. Mačky so závažnou neurologickou a okulárnou FIP neboli do štúdie prijaté. Skupina začala s GS-441524 v dávke 2,0 mg/kg SC q24h po dobu najmenej 12 týždňov, ktorá sa zvyšovala, keď to bolo indikované, na 4,0 mg/kg SC q24h.
Výsledky
Štyri z 31 mačiek, ktoré mali ťažkú formu ochorenia, uhynuli alebo boli eutanizované do 2-5 dní a piata mačka po 26 dňoch. Zvyšných 26 mačiek dokončilo plánovaných 12 alebo viac týždňov liečby. Osemnásť z týchto 26 mačiek zostáva zdravých v čase publikácie (OnlineFirst, február 2019) po jednom kole liečby, zatiaľ čo osem ďalších utrpelo relapsy choroby v priebehu 3–84 dní. Šesť z relapsov bolo neneurologických a dva neurologické. Tri z ôsmich ralapsujuúcich mačiek boli liečené opäť rovnakou dávkou, zatiaľ čo piatim mačkám bola dávka zvýšená z 2,0 na 4,0 mg/kg každých 24 hodín. Päť mačiek liečených druhýkrát vyššou dávkou, vrátane jednej s neurologickým ochorením, reagovalo dobre a v čase publikácie boli zdravé. Jedna z troch mačiek znovu liečených pôvodnou nižšou dávkou však mala relaps s neurologickým ochorením a bola eutanizovaná, zatiaľ čo dve zostávajúce mačky reagovali priaznivo, ale došlo k druhému relapsu. Tieto dve mačky boli úspešne liečené tretíkrát pri vyššej dávke, čo vo výsledku viedlo k 25 dlhodobo preživším mačkám. Jedna z 25 úspešne liečených mačiek bola následne eutanizovaná z dôvodu pravdepodobného nesúvisiaceho ochorenia srdca, zatiaľ čo 24 zostalo zdravých.
Záver a význam
GS-441524 sa ukázal ako bezpečný a efektívny pri liečbe FIP. Bola stanovená optimálna dávka 4,0 mg/kg SC q24h po dobu najmenej 12 týždňov.
Kľúčové slová: Nukleozidový analóg, GS-441524, infekčná peritonitída mačiek, FIP, klinická štúdia
Úvod
Lieky, ktoré inhibujú replikáciu vírusov, sa stali ústredným bodom zaujmu pri liečbe ľudských akútnych a chronických RNA a DNA infekcií. Vývoj záujmu o antivírusové lieky pre infekcie zvierat bol však oveľa pomalší. To platí najmä pre mačky, ktoré trpia niekoľkými chronickými vírusovými infekciami podobnými tým ľudským. Medzi infekčné činitele patrí vírus mačacej leukémie a imunodeficiencie (FeLV a FIV), mačací herpesvírus (FHV), virulentný systémový kalicivírus a koronavírus spôsobujúci mačaciu infekčnú peritonitídu (FIPV). Infekcie FeLV a FIV sa darí udržiavať pod kontrolou pomocou testovania, izolácie a/alebo očkovania. Ochorenie spojené s FHV bolo prvou mačacou vírusovou infekciou, kde bolo pre liečbu použité antivirotikum. Vysoko smrteľný systémový kalicivírus postihuje iba malý počet mačiek. Infekcia FIPV je najlepším kandidátom pre vývoj antivírusových liekov, pretože vakcíny sú neúčinné, prostredie s mnohými mačkami veľmi komplikuje prevenciu a zabíja 0,3–1,4% mačiek na celom svete.
Výskyt exotických chorôb, ako je ebola, stredovýchodný respiračný syndróm (MERS) a ťažký akútny respiračný syndróm (SARS) u ľudí, podnietil intenzívny výskum liekov, ktoré inhibujú replikáciu vírusu RNA. Jedným z najsľubnejších antivírusových liekov proti vznikajúcim RNA vírusom je proliečivo (prodrug) adenozínový nukleozidový monofosfát GS-5734 (Remdesivir; Gilead Sciences). GS-5734 preukázal účinnosť pri experimentálnej ebole u opíc rhesus a inhiboval epidemické aj zoonotické koronavírusy v tkanivových kultúrach a v myšacích infekčných modeloch. Tieto sľubné zistenia iniciovali výskum GS-5734 a jeho pôvodného nukleozidu GS-441524 proti FIPV infekcii mačiek. GS-441524 a GS-5734 majú porovnateľné hodnoty EC50 (1,0 uM) a CC50 (> 100 uM) proti FIPV v mačacích bunkách. Preto sa rozhodlo pre účely dalších testov s laboratórnymi mačkami zamerať na chemicky menej komplexný GS-441524. Farmakokinetická štúdia na dvoch laboratórnych mačkách preukázala trvalé a účinné plazmatické hladiny GS-441524 vyše 24 hodín po dávke podanej subkutánne (SC) alebo intravenózne (IV). Tieto výsledky sa rozšírili na 10 laboratórnych mačiek s experimentálne indukovanou brušnou efúznou mačacou infekčnou peritonitídou (FIP). Táto štúdia preukázala, že GS-441524 je vysoko účinný proti experimentálnej FIP, a otvorila tak cestu pre túto klinickú štúdiu.
Cieľom tejto štúdie bolo demonštrovať bezpečnosť a účinnosť GS-441524 pri liečbe mačiek s prirodzene sa vyskytujúcou FIP. Malomolekulárne lieky, ako je GS-441524, majú hmotnosť <900 daltonov a veľkosť približne 1 nm a môžu ľahko prenikať do buniek a interagovať s kľúčovými cieľovými molekulami. Na rozdiel od už publikovaných látok alebo liekov, ktoré inhibujú FIPV brzdením bunkových procesov vírusmi využívaných pre ich replikáciu, malé molekuly, ako je GS-441524, interferujú priamo s vírusom kódovanými replikačnými procesmi.
Materiály a metódy
Príprava lieku
GS-441524 poskytla spoločnosť Gilead Sciences ako čistý a vysoko stabilný prášok, ktorý bol zriedený na koncentráciu 10 alebo 15 mg/ml v 5% etanole, 30% propylénglykole, 45% PEG 400, 20% vode (pH 1,5 s HCI ). Roztok bol umiestnený do sterilných 50 ml sklenených injekčných fľaštičiek, v ktorých sa pretrepal až do rozpustenia a potom sa podrobil sonickej vodnej kúpeli na 5 až 20 minút, kým nebol číry. Zriedený liek bol uložený do chladu a bol použitý v priebehu 3–4 týždňov.
Koncepcia štúdie
Táto štúdia prebiehala podľa protokolov 19336 a 19863 schválených Inštitucionálnym výborom pre starostlivosť a použitie zvierat a Výborom pre hodnotenie klinických skúšok Komisie pre klinické skúšky veterinárnej lekárskej fakultnej nemocnice na Kalifornskej univerzite v Davise. Inštitucionálne pravidlá vylučujú použitie chorých mačiek z útulkov alebo z podobných zariadení, kvôli požiadavke legálneho vlastníctva/adopcie a zaobchádzania za špecifických podmienok so súhlasom majiteľa (doplňujúci materiál). Štúdia nezahŕňala kontrolnú skupinu, pretože neexistuje účinná zrovnávacia liečba. Nebola zahrnutá ani placebo skupina, pretože prípravné štúdie in vitro a in vivo naznačovali, že GS-441524 bude bezpečný a účinnejší ako žiadna liečba.
Výber prípadov a potvrdenie diagnózy
Mačky s FIP boli prijaté od majiteľov alebo ich veterinárnych lekárov, ktorí hľadali súčasné možnosti liečby alebo prístup k predchádzajúcej štúdii antivírusových liekov. Počiatočná diagnóza FIP bola založená predovšetkým na charakteristickej signalizácii, klinických anamnézach a príznakoch choroby, výsledkoch bežných laboratórnych testov a vyšetrení brušných alebo hrudných výpotkov. Definitívnejšia diagnóza založená na RT-PCR alebo imunohistochémii bola síce žiaduca, ale nebola nevyhnutnou podmienkou pre zaradenie. Mačky so zjavným očným alebo neurologickým ochorením boli vyradené kvôli pochybnostiam ohľadne schopnosti antivírusových liekov, vrátane GS-441524, preniknúť cez hematoencefalickú alebo hematookulárnu bariéru.
Do štúdie bolo prijatých 31 mačiek a ich majiteľov (tabuľka 1). Majitelia alebo zástupcovia 26 mačiek prišli na úvodnú liečbu priamo do UC Davis a päť majiteľov a ich mačky (CT59, CT73, CT76, CT78, CT80) boli v ošetrení miestneho veterinára. Mačky prítomné na UC Davis boli znovu prehodnotené, ich diagnóza FIP bola znovu potvrdená na základe signalizácie, klinickej anamnézy, fyzikálneho vyšetrenia, výsledkov predchádzajúcich laboratórnych testov a opakovania kompletného krvného obrazu (CBC), sérových bielkovín a analýz výpotkov. Hrudný alebo brušný výpotok u mačiek s vlhkou FIP bol potvrdený ako pozitívny na FIPV 7b RNA pomocou RT-PCR. Mačky so známkami neefúznej FIP boli ďalej testované brušnou a hrudnou ultrasonografiou na primárne lézie. Očné ochorenie bolo potvrdené oftalmologickou službou VMTH, UC Davis. Neurologický stav v prípadoch s možnými príznakmi ochorenia centrálneho nervového systému bol vyhodnocovaný neurologickou službou VMTH.
Tabuľka 1
Zoznam 31 mačiek zaradených do testovania vrátane laboratórneho označenia, mena mačky, plemena, klinickej formy infekčnej peritonitídy (FIP) a dátumu diagnózy
| ID | Meno | Dátum narodenia | Plemeno | Pohlavie | Pôvod | Dátum diagnózy | Forma FIP |
|---|---|---|---|---|---|---|---|
| CT52 | Luna | 9.1.2017 | Savannah | F | Chovateľ | 24.4.2017 | Brušná efúzna |
| CT53 | Ice Bear | 2.8.2016 | DLH | MC | Záchranná skupina | 5.5.2017 | Brušná efúzna |
| CT54 | Charolett | 11.7.2016 | Siberian | F | Chovateľ | 15.4.2017 | Brušná efúzna |
| CT55 | Dempsey | 26.6.2016 | DSH | MC | Záchranná skupina | 15.4.2017 | Brušná efúzna |
| CT56 | Mudsa | 1.7.2016 | DSH | MC | Útulok | 12.5.2017 | Brušná efúzna |
| CT57 | Boone | 31.10.2016 | DSH | FS | Záchranná skupina | 8.5.2017 | Brušná efúzna |
| CT58 | Justyna | 17.4.2016 | Ragdoll | F | Chovateľ | 25.5.2017 | Brušná efúzna |
| CT59 | Bubba | 11.4.2011 | DLH | MC | Túlavá | 10.4.2017 | Brušná neefúzna |
| CT60 | Joey | 25.7.2016 | DSH | MC | Záchranná skupina | 20.5.2017 | Brušná efúzna |
| CT61 | Hudson | 1.7.2016 | DSH | MC | Záchranná skupina | 29.5.2017 | Hrudná efúzna |
| CT62 | Luca | 10.3.2016 | DSH | MC | Záchranná skupina | 30.5.2017 | Brušná efúzna |
| CT63 | Bao Bao | 6.11.2016 | DSH | MC | Záchranná skupina | 3.6.2017 | Brušná efúzna |
| CT64 | Cedrick | 27.6.2016 | DSH | MC | Záchranná skupina | 22.5.2017 | Brušná neefúzna |
| CT65 | Mona | 14.3.2016 | Exotic SH/Persian | F | Chovateľ | 11.6.2017 | Hrudná efúzna |
| CT66 | Squeekers | 7.6.2016 | DSH | FS | Útulok | 14.6.2017 | Brušná efúzna |
| CT67 | Double | 2.3.2016 | Ragdoll | FS | Chovateľ | 20.6.2017 | Brušná efúzna |
| CT68 | Tuckerman | 8.5.2016 | Maine Coon | MC | Záchranná skupina | 22.6.2017 | Brušná efúzna |
| CT69 | Danny | 16.6.2015 | Snowshoe | MC | Útulok | 22.6.2017 | Hrudná efúzna |
| CT70 | Tolstoy | 1.8.2014 | DSH | MC | Záchranná skupina | 25.6.2017 | Brušná efúzna |
| CT71 | Amadeus | 29.6.2016 | DSH | MC | Túlavá | 20.6.2017 | Hrudná efúzna |
| CT72 | Bella | 25.2.2017 | British SH | F | Chovateľ | 20.6.2017 | Brušná efúzna |
| CT73 | Siersha | 8.8.2015 | DSH | FS | Útulok | 21.6.2017 | Brušná neefúzna |
| CT74 | Maive | 4.3.2017 | Siberian | FS | Chovateľ | 7.7.2017 | Brušná efúzna |
| CT75 | Lucy | 31.3.2017 | DSH | F | Záchranná skupina | 10.7.2017 | Brušná efúzna |
| CT76 | Pie | 20.7.2016 | Exotic SH | M | Chovateľ | 28.6.2017 | Brušná efúzna |
| CT77 | Mila | 15.3.2017 | Siberian | FS | Chovateľ | 3.7.2017 | Brušná efúzna |
| CT78 | Polly | 1.3.2016 | DSH | MC | Záchranná skupina | 22.7.2017 | Brušná neefúzna |
| CT79 | Oona | 21.9.2016 | Himalayan | F | Chovateľ | 18.7.2017 | Hrudná neefúzna |
| CT80 | Fezzik | 17.10.2016 | DLH | MC | Túlavá | 25.7.2017 | Brušná efúzna |
| CT81 | Jewelkat | 8.9.2016 | Persian | FS | Chovateľ | 1.8.2017 | Hrudná efúzna |
| CT82 | Tiko | 8.4.2016 | DSH | MC | Záchranná skupina | 6.8.2017 | Brušná efúzna |
Liečebný režim
Na základe predchádzajúcich experimentov s tkanivovými kultúrami a farmakokinetických štúdií na laboratórnych mačkách bol počiatočný dávkovací režim pre GS-441524 stanovený na 2,0 mg/kg SC q24h. Na základe skúseností s inhibítorom 3CL proteázy GC376 proti prirodzene sa vyskytujúcej FIP bola určená minimálna doba liečby 12 týždňov. Liečba sa predĺžila o jeden alebo viac týždňov u mačiek, ktoré stále mali abnormálne hodnoty sérových bielkovín. V neskorších štádiách štúdie sa dávka zvýšila z 2,0 na 4,0 mg/kg v prípadoch, keď sa liečba musela predĺžiť, alebo keď došlo k relapsu choroby. Majiteľom bola každé 4 týždne zasielaná nová dávka lieku vo forme vopred natiahnutých injekčných striekačiek Luer lock s objemom 1 alebo 3 ml s 1 palcovými ihlami Luer veľkosti 22G (0,7x25mm). Injekčné striekačky sa uložili do chladničky a pred aplikáciou sa zahriali na izbovú teplotu. Injekcie boli aplikované pozdĺž chrbtice od 2 cm za lopatkami do polovice bedrovej oblasti a do polovice vzdialenosti nadol na susedný hrudník a boky.
Monitorovanie počas počiatočného obdobia liečby
V čase vstupu do testovania bola u mačiek vysadená všetka liečba, ktorá nebola nevyhnutná – antibiotiká, kortikosteroidy, interferóny, pentoxifylín, nesteroidné protizápalové lieky, alebo lieky na tlmenie bolesti. Počas pobytu na UC Davis boli mačky každých 12 hodín monitorované z hľadiska teploty, chuti do jedla, aktivity, močenia a defekácie. Krv bola odoberaná v 1–3 denných intervaloch na vyhodnotenie hematokritu, celkového proteínu, bilirubínu, počtu bielych krviniek a diferenciálneho počtu bielych krviniek.
Vzorky ascitu sa odobrali na začiatku a potom sa odoberali v jedno alebo niekoľko denných intervaloch čo najdlhšie, ako to bolo možné, a testovali sa na úrovne prepisov FIPV 7b RNA kvantitatívnou (q) RT-PCR (IDEXX molekulárna diagnostika). Rezy tkaniva fixovaného formalínom od piatich pitvaných mačiek, boli podrobené imunohistochémii na proteín nukleokapsidy FIPV.
Monitorovanie počiatočnej a dlhodobej reakcie na liečbu
Mačky boli prepustené do domáceho ošetrenia, keď bola zaznamenaná významná priaznivá odpoveď na liečbu, zvyčajne do 3–5 dní. Počas tohto obdobia boli majitelia poučení, ako správne podávať subkutánne injekcie, a boli vyzvaní, aby pokračovali v denných záznamoch o telesnej teplote, aktivite, chuti do jedla, defekácii a močení a týždenných meraniach telesnej hmotnosti. CBC a sérový chemický panel boli robené v mesačných intervaloch miestnymi veterinármi alebo počas návštev VMTH. Bolo potrebné zaznamenávať a okamžite hlásiť akékoľvek abnormálne príznaky alebo správanie. Odôvodnená eutanázia bola zvyčajne vykonaná veterinárnym lekárom majiteľa alebo, ak to bolo možné, v UC Davis. Telá boli okamžite ochladené a zapečatené v plastových vreciach, a odoslané do 2 alebo menej dní v kontajneroch chladených ľadom na UC Davis expresnou poštou. Pitvy boli vykonané jedným z autorov (ML) v Anatomic Pathology Service, School of Veterinary Medicine, UC Davis. Bola rešpektovaná žiadosť majiteľa o konečnú dispozíciu tela.
Výsledky
Signalizácia a prezentácia choroby
Do štúdie bolo zaradených 31 mačiek vo veku od 3,4 do 73 mesiacov (priemerne 13,6 mesiacov) (tabuľka 1). Osemnásť mačiek boli domáce krátkosrsté a dlhosrsté , 13 mačiek predstavovalo zástupcov 10 rôznych plemien (tabuľka 1). Domáce mačky boli adoptované z organizácií na záchranu mačiek (n = 13), útulkov (n = 2) alebo to boli túlavé mačky z okolia (n = 3). Štúdia zahŕňala 14 samíc (7 nekastrovaných; 7 kastrovaných) a 17 samcov (1 nekastrovaný; 16 kastrovaných).
Dvadsaťšesť z 31 mačiek malo vlhkú FIP (6 hrudná, 20 brušná). Päť mačiek malo neefúznu FIP; štyri z nich (CT59, CT64, CT73, CT78) s ochorením lokalizovaným do brucha (mezenterické a ileo/cekálne/kolické lymfatické uzliny) a jedna (CT79) do hrudníka (pľúca, hilárne lymfatické uzliny) (tabuľka 1). Štyri ďalšie mačky vykazovali znaky skoršej suchej FIP, ktorá prešla do efúznej formy (CT57, CT65, CT67, CT71) (tabuľka 1). Hrubé príznaky očného ochorenia zodpovedajúce FIP sa potvrdili oftalmoskopickým vyšetrením u troch z 31 mačiek (CT56, CT65, CT71). Dve mačky (CT71, CT80) neochotne alebo už vôbec nedokázali skákať na vyvýšené miesta, čo naznačovalo neurologické postihnutie.
Výsledky liečby
Štyri mačky boli eutanizované (CT62, CT72, CT75) alebo uhynuli (CT56) počas prvých 2–5 dní kvôli závažnému ochoreniu a iným komplikáciám a piata mačka bola eutanizovaná (CT54) po 26 dňoch z dôvodu chýbajúcej reakcie na liečbu (obrázok 1). Liečba prebiehala bez prerušenia, s výnimkou troch mačiek, ktorým bol v 4. (mačka CT80) alebo 8. týždni (mačky CT53, CT71) poskytnutý dvojtýždňový oddych kvôli problémom s podávaním injekcií a kožným reakciám (obrázok 1). Mačka CT53 bola po druhom relapse liečená po dobu 8 a nie 12 týždňov z dôvodu zvýšenia močoviny v krvi a zvýšenia sérových hladín symetrického dimetylarginínu (SDMA).

Časová škála liečby a klinický výsledok 31 mačiek, ktoré boli zaradené do klinickej štúdie GS-441524. Obdobie liečby je označené plnou čiarou (dávka 2 mg/kg) alebo prerušovanou čiarou (dávka 4 mg/kg). Hviezdičky označujú bod relapsu. Dátum ukončenia liečby pre mačky, ktoré dosiahli trvalú klinickú remisiu, je uvedený v zátvorkách. Časový bod a príčina smrti sú označené krížikom
Klinická reakcia 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby, bola dramatická. Horúčka zvyčajne ustúpila do 12–36 hodín (obrázok 2), súčasne s každodenným výrazným zvýšovaním chute do jedla, úrovne aktivity a prírastku hmotnosti. Brušné výpotky rýchlo vymizli počas 1-2 týždňov, počnúc asi 10.-14. dňom po zahájení liečby. Mačky s hrudným výpotkom zvyčajne vykazujúce dýchavičnosť, absolvovali u praktickych súkromných veterinárov odsatie pleurálnych výpotkov ešte pred príchodom na UC Davis. Zbytková dýchavičnosť a hrudný výpotok rýchlo reagovali na liečbu a po 7 dňoch už neboli vôbec viditeľné. Žltačka pomaly odznela v priebehu 2–4 týždňov, súčasne s poklesom hyperbilirubinémie. Známky očného ochorenia začali miznúť do 24-48 hodín a prestali byť zjavné navonok i pre oftalmoskopické vyšetrenie do 7–14 dní. V priebehu liečby začalo dochádzať k zmenšovaniu zväčšených mezenterických a ileo/cekálno/kolických lymfatických uzlín. Všetkých 26 mačiek vyzeralo podľa odhadov majiteľov navonok normálne alebo takmer normálne po 2 týždňoch liečby. Po 2 týždňoch liečby sa kládol dôraz na sledovanie niekoľkých parametrov krvných testov. Kľúčové hodnoty zahŕňali hematokrit, celkový počet bielych krviniek, absolútny počet lymfocytov, celkový sérový proteín, sérový globulín, sérový albumín a pomer albumín: globulín (A:G).

Priemer (plná čiara) a 1 SD (smerodajná odchýlka) (čiarkovane) telesných teplôt počas prvých 5 dní liečby GS-441524. Normálny teplotný rozsah pre mačky je 37,7–39,1 °C (100–102,5 ° F). Teploty klesli do normálneho rozsahu do 12–36 hodín od začiatku liečby
Osemnásť z 26 mačiek, ktoré absolvovali najmenej 12 týždňov neprerušenej primárnej liečby, nevyžadovalo žiadnu ďalšiu liečbu. Osem ďalších mačiek však utrpelo relapsy choroby v priebehu 3–84 dní (priemerne 23 dní) (obrázok 1). Táto skupina zahŕňala tri mačky, u ktorých došlo k dočasnému prerušeniu počiatočnej liečby (CT53, CT71, CT80), a päť mačiek (CT53, CT57, CT60, CT68, CT73), ktoré vyžadovali predĺženú primárnu liečbu (obrázok 1). Relapsy choroby u 2/8 mačiek (CT57, CT71) mali zjavne neurologický charakter s vysokou horúčkou a silnou zadnou ataxiou a nekoordináciou, zatiaľ čo relapsy choroby u zvyšných šiestich mačiek pozostávali hlavne z horúčky, anorexie a znízenej aktivity. Iba jedna mačka (CT60) mala pri relapse zjavný brušný výpotok. Jedna mačka (CT57) bola eutanizovaná 2 týždne po relapse s neurologickými príznakmi, ktoré nereagovali na druhé kolo liečby.
U ôsmich mačiek bolo rozhodnuté zvýšiť dávku GS-441524 z 2,0 na 4,0 mg/kg, buď z dôvodu predĺženia liečby (CT77, CT80), alebo z dôvodu jedného (CT60, CT68, CT71, CT73) alebo dvoch relapsov (CT53, CT63), alebo preto, že relaps mal neurologickú formu (CT71). Všetkých osem mačiek reagovalo pozitívne na režim zvýšeného dávkovania.
Celkovo 25/26 mačiek liečených 12 týždňov alebo dlhšie dosiahlo trvalú remisiu FIP, hoci jedna z nich následne zomrela na nesúvisiaci problém so srdcom (pozri „Pitevné nálezy“). Najdlhšie prežívajúce mačky v čase publikácie (OnlineFirst, február 2019) ukončili liečbu v auguste 2017 a najkratšie v máji 2018, všetky po ukončení pozorovacieho obdobia, v ktorom ešte mohlo dôjsť k relapsu (tj. 84 dní po ukončení liečby). 24 preživších mačiek bude starostlivo monitorovaných pre prípadný návrat príznakov ochorenia a budú sa pravidelne testovať na celkový pomer bielkovín, globulínu, albumínu a A:G počas prvého roka. Menej intenzívne monitorovanie sa bude vykonávať po zvyšok života mačiek. Majitelia boli upozornení, aby sa vyhli zbytočnému namáhaniu mačiek počas prvých 3 mesiacov, aj keď štyri mačky (CT52, CT58, CT65, CT79) a jeden kocúr (CT76) absolvovali bezproblémovú kastráciu.
Ukazovatele priaznivej reakcie na liečbu
Najjednoduchším dlhodobým meradlom účinnosti liečby bola telesná hmotnosť. K nárastu hmotnosti o 20–120% došlo počas a po liečbe, dokonca aj u mačiek, ktoré v čase diagnózy mali 1 rok alebo viac. Zdá, že výrazný rast sa prejavil aj u mladších mačiek, ako to nezávisle zaznamenali ich majitelia. Tieto výrazné zrýchlenia rastu po liečbe naznačili, že FIP bola u mnohých mačiek nejaký čas pred diagnózou subklinická a ovplyvnila ich rast. Pri sledovaní neskorších účinkov liečby a pri pozorovaní možných toxicít liekov sa osvedčili aj CBC (hematológia) a chemický profil (biochémia).
CBCs (Hematológia)
Mačky vykazovali zvýšený počet bielych krviniek, ktorý klesol na normálne hodnoty v priebehu prvých 2 týždňov liečby (obrázok 3a). Lymfopénia zaznamenaná v čase prijatia vymizla počas prvého týždňa liečby (obrázok 3b). Pri prijatí sa pozorovala mierna až stredne závažná anémia, čo sa prejavilo v hematokrite (PCV) (obrázok 4). Hematokrit sa vrátil na normálne hodnoty až po 6–8 týždňoch liečby. Absolútny celkový počet bielych krviniek a lymfocytov boli jedinými významnými hodnotami počas prvého týždňa liečby, zatiaľ čo PCV poskytol presnejší obraz postupu liečby počas prvých 8 týždňov.
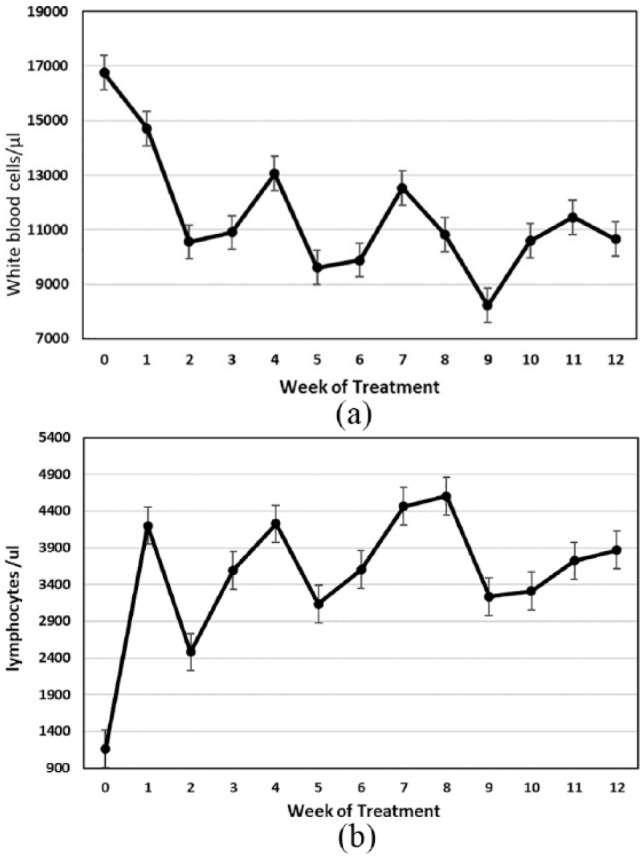
(a) Priemerný počet bielych krviniek so štandardnou odchýlkou u 26 mačiek, ktoré dokončili primárny liečebný režim 12 alebo viac týždňov. (b) Priemerný absolútny počet lymfocytov v krvi so štandardnou odchýlkou u 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby

Hematokrit (PCV) so štandardnou odchýlkou pre 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby. Bodkovaná čiara naznačuje trend rastu PCV v priebehu času
Zmeny sérových bielkovín
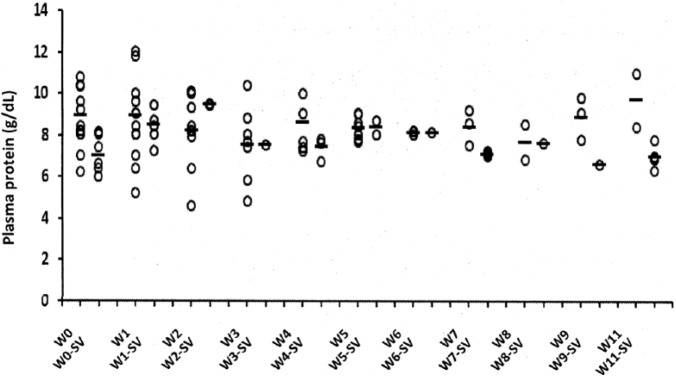
Mačky s FIP často vykazovali vyššiu ako normálnu celkovú koncentráciu bielkovín v sére, vysokú hladinu sérového globulínu, nízku hladinu sérového albumínu a nízky pomer A:G (obrázky 5–7). Abnormálne hodnoty sérových bielkovín sa progresívne zlepšovali a dosiahli normálne hodnoty po 8–10 týždňoch liečby (obrázky 5–7). Hladina celkového proteínu bola najmenej informatívna, čo naznačuje nízka hodnota R2 (0,1883) trendovej spojnice (obrázok 5). Avšak 3 týždne po zahájení liečby došlo k dramatickému a prechodnému zvýšeniu celkových hladín proteínov (obrázok 5). Tento jav súvisel so zvýšením sérových globulínov (obrázok 6a) v čase rýchleho ústupu brušných výpotkov.

Priemerné hladiny celkového proteínu v sére a štandardná odchýlka pre 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby

(a) Priemerné hladiny sérového globulínu a štandardná odchýlka pre 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby. (b) Priemerné hladiny sérového albumínu a štandardná odchýlka pre 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby

Priemerné pomery albumínu:globulínu (A/G) a štandardná odchýlka pre 26 mačiek, ktoré absolvovali najmenej 12 týždňov liečby
Plazmatické hladiny globulínu stúpali počas prvých 3 týždňov liečby, dosiahli vrchol a potom pomaly klesali na maximálnu referenčnú hodnotu 4,5 g/dl alebo nižšiu do 9. týždňa (obrázok 6a). Aj keď sa zdá, že hladiny globulínu v priebehu času reflektovali stav liečby, nízka hodnota R2 (0,3621) ukázala, že sa jedná o menej spoľahlivý ukazovateľ pokroku v liečbe.
Hladiny albumínu v sére 26 mačiek liečených najmenej 12 týždňov boli v čase zahájenia liečby zvyčajne nízke (⩽3,2 g/dl) (obrázok 6b). Hladiny albumínu sa potom pomaly zvyšovali a dosiahli normálnu úroveň po 8 týždňoch. Trendová čiara tohto nárastu albumínu mala vysokú hodnotu R2 (0,79), vďaka čomu boli hladiny sérového albumínu, ako aj PCV, dobrým indikátorom pokroku v liečbe. Ako sa očakávalo, pomer A:G vykazoval v priebehu času rovnako silnú trendovú líniu a okolo 8. týždňa liečby úroveň presiahla hodnotu 0,70 (obrázok 7).
Pokles hladiny vírusovej RNA v bunkách z ascitickej tekutiny v spojitosti s liečbou
Počas prvých 2–9 dní antivírusovej liečby sa odoberali od ôsmich mačiek sekvenčné vzorky ascitu a testovali sa na hladiny vírusovej RNA pomocou qRT-PCR (tabuľka 2). Najspoľahlivejším zdrojom FIPV RNA boli celé výpotky alebo ich bunkové frakcie. U 7/8 mačiek hladiny vírusovej RNA poklesli do 2-5 dní, často na nedetekovateľné hodnoty. U jednej mačky (CT54) sa neprejavil významný pokles hladín vírusovej RNA ani v priebehu 9 dní.
Tabuľka 2
Úrovne prepisov RNA vírusu mačacej infekčnej peritonitídy 7b v celých ascitoch alebo v bunkovej frakcii ascitickej tekutiny počas počiatočnej liečby GS-441524
| ID vzorky | Dni liečby | Typ vzorky | Kópie vírusovej RNA/ml |
|---|---|---|---|
| CT52 | 0 | Ascites | 9.44 × 104 |
| 3 | Ascites | Nezistiteľné | |
| CT54 | 0 | Ascites | 8.49 × 105 |
| 2 | Ascites | 6.97 × 104 | |
| 4 | Ascites | 2.44 × 103 | |
| 7 | Ascites | 2.07 × 103 | |
| 9 | Ascites | 6.46 × 104 | |
| CT62 | 0 | Ascites | 5.96 × 103 |
| 2 | Ascites | 1.53 × 103 | |
| 8 | Ascites | Nezistiteľné | |
| CT74 | 0 | Bunky | 6.51 × 106 |
| 2 | Bunky | 3.39 × 105 | |
| CT75 | 0 | Bunky | 9.08 × 106 |
| 3 | Bunky | 4.75 × 105 | |
| 4 | Bunky | 2.50 × 105 | |
| CT77 | 0 | Ascites | 5.47 × 104 |
| 2 | Ascites | 3.93 × 103 | |
| CT80 | 0 | Ascites | 4.10 × 103 |
| 2 | Ascites | Nezistiteľné | |
| CT82 | 0 | Ascites | 1.13 × 104 |
| 5 | Ascites | Nezistiteľné |
Vedľajšie účinky pozorované počas liečby a po liečbe
Ohraničené reakcie v mieste vpichu. Boli pozorované dva typy reakcií v mieste vpichu, a či boli spôsobené liekom, riedidlom alebo obomi, nebolo zistené. Okamžité reakcie na bolesť sa prejavovali vokalizáciou, občasným vrčaním a posturálnymi zmenami trvajúcimi 30–60 s. Tieto počiatočné reakcie sa časom zmierňovali, pretože majitelia sa stávali viac zručnými v podávaní injekcií a mačky sa tejto rutine postupne prispôsobovali. U šestnástich z 26 liečených mačiek sa prejavili reakcie v mieste vpichu (tabuľka 3). Reakcie boli zjavné najčastejšie počas prvých 4 týždňov a progredovali do otvorených rán iba u 7/16 mačiek. Ulcerácie sa zahojili do 2 týždňov zastrihnutím okolitých chlpov a jemným vyčistením rany vatovým tampónom namočeným v jednom diele peroxidu vodíka pre domácnosť a v dvoch dieloch vody dvakrát denne. Iba tri mačky mali znateľné jazvy v miestach vpichu.
Tabuľka 3
Reakcie v mieste vpichu u 16 z 26 mačiek liečených GS-441524 po dobu 12 týždňov alebo dlhšie
| ID mačky | Povrchové lézie | Otvorené rany | Jazvy |
|---|---|---|---|
| CT53 | 3 | 1 | 0 |
| CT58 | 1 | 0 | 0 |
| CT60 | 0 | 0 | 2 |
| CT61 | 5 | 0 | 0 |
| CT63 | 2 | 2 | 0 |
| CT64 | 1 | 0 | 1 |
| CT65 | 9 | 1 | 1 |
| CT66 | 3 | 2 | 0 |
| CT68 | 4 | 0 | 0 |
| CT71 | 5 | 1 | 0 |
| CT73 | 7 | 1 | 0 |
| CT74 | 3 | 1 | 0 |
| CT76 | 10 | 0 | 0 |
| CT78 | 7 | 0 | 0 |
| CT79 | 2 | 0 | 0 |
| CT82 | 2 | 0 | 0 |
Systémové liekové reakcie. Liečba GS-441524 v celkovom období 12–30 týždňov bola pozoruhodne bezpečná. V hodnotách CBC neboli pozorované žiadne dlhodobé abnormality (obrázky 3 a 4). Testy funkcie pečene a obličiek a hladiny amylázy/lipázy zostali počas liečby a po liečbe normálne (doplňujúce obrázky S1 – S3). Jedinou výnimkou bola mačka CT53, u ktorej došlo k progresívnemu zvýšeniu močoviny v krvi (BUN) na 35 mg/dl (referenčný interval [RI] 16–37 µg/dl) a k náhlemu zvýšeniu SDMA (20 µg/dl) (RI 0-14 µg/dl) po 8 týždňoch v treťom kole liečby v režime zvýšenej dávky 4 mg/kg. Aj keď mali tieto príznaky stále miernu povahu, bolo pre istotu rozhodnuté ukončiť liečbu. Tieto abnormality pri testovaní o 1 mesiac neskôr už neboli prítomné a mačka je momentálne v remisii choroby.
Pitevné nálezy
Štyri mačky (CT56, CT62, CT72, CT75) boli eutanizované alebo uhynuli do 2–5 dní od zaradenia do štúdie a pitvy boli vykonané u všetkých okrem mačky CT75. Piata mačka (mačka CT54) bola eutanizovaná po 26 dňoch liečby. Všetkých päť týchto mačiek malo závažné brušné efúzne ochorenie. U mačky CT54 a CT56 sa pri pitve našli dôkazy o rozšírenej pyogranulomatóznej vaskulitíde zahŕňajúcej brušné vnútornosti, centrálny nervový systém a oči. U mačky CT56 došlo aj kompromitácii ileálnej steny v oblasti hustého infiltrátu a sekundárnej bakteriálnej sepse. Mačka CT72 mala ťažkú pyogranulomatóznu vaskulitídu obmedzenú na brucho so stredne ťažkým až ťažkým periférnym edémom a mineralizáciou kôry nadobličiek. Mačka CT62 trpela ťažkou pyogranulomatóznou a fibrinosuppuratívnou peritonitídou, ktorú komplikovala akútna perforácia žalúdka spojená s rastlinným materiálom a intralezionálnymi baktériami svedčiacimi o sepse. Mačka CT75 vykazovala chronickú formu FIP charakterizovanú silným spomalením rastu, masívne nízkym obsahom bielkovín / nízkym obsahom buniek vo výpotku, zrýchlenou činnosťou srdca svedčiacou o poškodení srdcovej funkcie a stredne závažným periférnym edémom. Echokardiogram ukázal bilaterálne zväčšenie predsiení, ale nijaký náznak primárneho srdcového ochorenia. Zdalo sa, že mačka reagovala na GS-441524 a bola prepustená. Mačka upadla o 2 dni neskôr do šoku a bola eutanizovaná bez pitvy.
V čase pitvy mačiek CT56, CT72 a CT75 pri použití qRT-PCR nebol vírus FIPV detekovaný, hoci vzorky ascitu pred liečbou boli pozitívne. Ascites z mačky CT54 vykazoval pozitívny výsledok qRT-PCR počas celej liečby (tabuľka 2) a tkanivá boli v čase pitvy stále imunohistochemicky pozitívne.
Po úspešnom absolvovaní jedného alebo viacerých kôl liečby boli eutanizované aj ďalšie dve mačky. Mačka CT57 bola po jednom kole liečby normálna, ale o 2 týždne neskôr došlo k relapsu so závažnými neurologickými príznakmi. Mačka nereagovala na opakovanú liečbu a bola usmrtená. Lézie typické pre FIP sa našli v mozgu a bruchu, ale boli negatívne na FIPV určený imunohistochémiou pre nukleokapsidový proteín alebo na 7b RNA pomocou qRT-PCR. Mačka CT80 bola úspešne liečená na efúznu brušnú FIP, ale o 4 týždne neskôr sa u nej objavili silné bolesti zadných nôh a krížov. Zistilo sa, že mačka mala výrazné zhrubnutie steny ľavej komory a septa, ktoré spôsobilo vážne zúženie komory (obrázok 8). Mikroskopický vzhľad steny ľavej srdcovej komory bol typický pre vrodenú mačaciu hypertrofickú kardiomyopatiu (HCM). V brušnej dutine, na hrudníku, v očiach, v mozgu alebo v chrbtici sa nezistili žiadne hrubé ani mikroskopické lézie FIP a qRT-PCR nedetekoval FIPV antigén a ani RNA FIPV.

Prierez srdcom mačky CT80 vykazujúci extrémnu hypertrofiu steny ľavej komory a septa a extrémne zúženie komory
Diskusia
GS-441524 je za posledné 2-3 roky po GC376 druhým testovaným cieleným antivírusovým liekom pre liečbu FIP. Tieto dva lieky inhibujú vírusovú replikáciu dvoma veľmi odlišnými spôsobmi, buď ukončením vírusovej RNA transkripcie alebo blokovaním štiepenia vírusového polyproteínu. Oba procesy sú dobre známym cieľom pre liečbu niektorých ľudských vírusových ochorení. Kľúčovou otázkou je porovnanie liečby nukleozidovým analógom s liečbou inhibítorom vírusovej proteázy. Tieto dva lieky poskytli prakticky identické výsledky v štúdiách na tkanivových kultúrach a experimentálne infikovaných mačkách. Účinnosť proti prirodzene sa vyskytujúcej FIP sa však javila pri GS-441524 vyššia ako pri GC376. Šesť z 20 mačiek liečených GC376 zostáva dodnes v remisii (Pedersen NC, nepublikované údaje, 2018) v porovnaní s 25/31 mačkami liečenými GS-441524. Ochorenia, ktoré nereagovali na opakovanú liečbu, sa vyskytli u 14/20 mačiek s GC376 ale iba u jednej mačky liečenej GS-441524. 8 zo 14 relapsov spojených s GC376 malo neurologický charakter, v porovnaní s 2/8 relapsmi s GS-441524. Jeden z dvoch neurologických relapsov u mačiek liečených GS-441524 reagoval na opakovanú liečbu vyššou dávkou, zatiaľ čo neurologické relapsy s GC376, dokonca ani pri zvýšenej dávke, už neboli liečiteľné. Obidve liečby spôsobovali podobné reakcie v mieste vpichu. Obidva lieky sa javia ako pomerne bezpečné, hoci GC376 interferoval s vývojom trvalých zubov, keď sa podával mladším mačiatkam.
Aj keď sa zdá, že výsledky klinickej štúdie uprednostňujú GS-441524, niektoré rozdiely mohli byť ovplyvnené tým, ako boli tieto dva lieky podávané. Účinnosť GC376 sa mohla zlepšiť, ak by bolo všetkých 20 mačiek liečených bez prerušenia po dobu 12 týždňov, namiesto toho, aby boli liečené progresívne dlhšími obdobiami, začínajúcimi iba na 2 týždňoch. Päť zo šiestich mačiek vyliečených pomocou GC376 patrilo medzi sedem mačiek, ktoré boli liečené nepretržite po dobu 12 týždňov, zatiaľ čo bola vyliečená iba jedna z 13 mačiek liečených jedenkrát alebo viackrát po kratšiu dobu. Tieto kratšie doby trvania liečby boli nevyhnutné na stanovenie 12-týždňového obdobia použitého pre všetky mačky v tejto štúdii. Klinická štúdia GC376 okrem toho zahŕňala menej mačiek a bola limitovaná obmedzeným prísunom lieku, čo sťažilo testovanie ďalších dávkovacích režimov. Preto by sa mal GC376 pred akýmkoľvek konečným porovnaním ďalej študovať s použitím minimálne 12 týždňov s vyššou dávkou a väčším počtom mačiek. Bolo by tiež dôležité niekedy v budúcnosti vyhodnotiť obidva typy liekov v kombinácii, tak ako sa to robí pri HIV/AIDS a hepatitíde C.
V každej štúdii tohto typu treba počítať s predčasnými úmrtiami, ale ako by sa mali posudzovať pri analýze účinnosti? Päť predčasných úmrtí v tejto štúdii bolo zahrnutých do analýzy účinnosti GS-441524, ale boli vyradené v štúdii GC376. Pre zahrnutie úmrtí do štúdie je dôležité zistenie statusu vírusu v čase smrti. Vírusová RNA sa nezistila u troch pitvaných mačiek, ktoré uhynuli po 2–5 dňoch liečby s GS-441524, čo naznačuje, že liek bol účinný, ale choroba bola v príliš pokročilom štádiu. Nebolo to tak v prípade štvrtej pitvanej mačky, ktorá prežila 26 dní; hladiny vírusovej RNA počas celého obdobia liečby neklesli a príznaky choroby sa nezmiernili. Preto je možné, že táto mačka uhynula v dôsledku neúspešného zastavenia replikácie vírusu. Rezistencia na GS-5734 (Remdesivir), proliečivo GS-441524, bola spojená s mutáciami aminokyselín v RNA polymeráze a korekčnou exonukleázou v tkanivovými kultúrami propagovaných koronavírusoch. Či sa u tejto mačky vyskytla podobná rezistencia, bude ešte treba zistiť. Rezistencia na lieky bola pozorovaná u aj u jednej mačky v teste GC376. Našťastie žiadna z ďalších mačiek v súčasnej štúdii nevykazovala príznaky rezistencie na lieky. U budúcich mačiek, ktoré nereagujú vôbec alebo reagujú nedostatočne na primárnu alebo sekundárnu liečbu, je však potrebné túto možnosť vziať do úvahy.
Počiatočná dávka GS-441524 použitá v predloženej štúdii bola stanovená na základe predchádzajúcich farmakokinetických a experimentálnych infekčných štúdií s laboratórnymi mačkami. Tieto štúdie naznačili, že 2,0 a 5,0 mg/kg SC q24h po dobu 14 dní by boli rovnako účinné aj pri klinickej štúdii. Preto bola pre klinické testovanie zvolená dávka 2,0 mg/kg, pretože by to znížilo spotrebu lieku o 60%. Aj keď bolo toto rozhodnutie potvrdené u 18/26 mačiek, osem ďalších mačiek buď utrpelo relapsy choroby (dve dokonca dvarát), alebo si vyžiadali dlhšie trvanie liečby, aby sa kľúčové hodnoty krvi dostali späť do normálu. Preto bolo urobené rozhodnutie zvýšiť dávku GS-441524 z 2,0 mg/kg na 4,0 mg kg SC q24h u mačiek, u ktorých došlo k relapsu alebo vyžadovali predĺženú liečbu. Úspešnosť 4,0 mg/kg SC q24h u najmenej 12 takýchto mačiek, ako aj u jednej mačky s neurologickým ochorením, nás priviedla k záveru, že ide o účinnejšie dávkovanie a malo by sa stať základom pre budúcu liečbu.
Bolo dôležité sledovať jednoduché biologické ukazovatele pokroku v priebehu ⩾ 12 týždňovej liečby. Ako užitočné markery boli identifikované hladiny HCT (PCV), hladiny celkového proteínu v sére, globulínu a albumínu a pomer A:G. Na základe týchto parametrov sa ukázalo, že mačky sa po 6–10 týždňoch liečby ešte celkom nezotavili. Toto zistenie potvrdilo minimálne 12-týždňové trvanie liečby stanovené v predchádzajúcej klinickej štúdii GC376. Chronická anémia (anémia zápalu) postihuje 18–95% ľudí s akútnymi a chronickými infekciami a je normocytová/normochromická a nesúvisí s nedostatkom železa. Dobrým ukazovateľom aktivity ochorenia boli aj plazmatické hladiny albumínu, a je známe, že nízky albumín a nízky HCT (PCV) korešpondujú s výskytom chronického ochorenia. Hyperglobulinémia u mačiek s FIP bola klasifikovaná ako infekčná/zápalová a je spôsobená zvýšením vo všetkých triedach gama globulínov a variabilnými prírastkami vo frakcii alfa-2 globulínov. Výrazná tendencia mačiek s FIP k vysokej sérovej hladine globulínu a nízkej hladine albumínu robí z pomeru A:G obzvlášť dobrý indikátor aktivity ochorenia.
Očakávalo sa, že čistokrvné mačky nebudú rovnako dobre reagovať na liečbu z dôvodu geneticky oslabenej schopnosti imunologicky reagovať na FIPV, a že mladšie mačky s vlhkou FIP budú na liečbu reagovať najlepšie. V tejto štúdii však nakoniec čistokrvné mačky reagovali rovnako dobre ako obyčajné mačky, a plemená zastúpené mačkami v štúdii odrážali najpopulárnejšie súčasné plemená. Staršie mačky a mačky s čistou neefúznou FIP reagovali na liečbu GS-441524 rovnako dobre, ako mladé mačky a mačky s vlhkou FIP. Za predpokladu, že sa dá pomocou GS-441524 liečiť aj časť mačiek s očným a neurologickým ochorením, sa dá povedať, že by sa už žiadne prejavy FIP nemuseli považovať za neliečiteľné.
Bezpečnostný profil GS-441524 bol pôsobivý. Na základe CBC a sérových chemických hodnôt počas celkových liečebných období v trvaní od 12 do 30 týždňov sa až na jednu možnú výnimku nepozorovali žiadne významné systémové príznaky toxicity. Jedna mačka (CT53) mala mierny nárast BUN a SDMA v 8. týždni tretieho kola liečby a v rámci preventívnych opatrení si vynútila pozastavenie liečby. Na základe predchádzajúcich skúseností s GC376 boli obavy z účinku GS-441524 na vývoj trvalého chrupu. Tri mačky (CT52, CT74, CT77) v tejto štúdii boli vo veku 4 mesiacov alebo mladšie a stále mali juvenilný chrup a žiadna z nich nevykazovala žiadne následné zubnej abnormality. U GS-441524 sa pozorovali reakcie v mieste vpichu, ale ich počet bol pozoruhodne nízky a boli ľahko liečiteľné. Nezistilo sa, či je na vine liek, riedidlo alebo oboje. pH riedidla 1,5 bolo hlboko pod minimálnou hraničnou hodnotou 4,5 stanovenou FDA (Food and Drug Administration), avšak liečivá tohto typu sa ťažko rozpúštajú a stabilizujú pri fyziologicky priaznivejšom pH. Napriek tomu by sa malo vyhodnotiť viac fyziologických riedidiel.
Jedna mačka v štúdii (CT80) mala znepokojivé klinické príznaky. Aj keď mačka vykazovala efúznu brušnú FIP, mala aj dlhodobé príznaky nejasného zakrivenia zadnej končatiny, bolesti krížov, pravidelných epizód padania, neochoty skákať na vyššie miesta a nevysvetliteľných a prechodných zmien správania. Tieto príznaky viedli k liečbe mačky ešte dlho po zmiznutí brušného výpotku. Nakoniec sa prijalo rozhodnutie liečbu prerušiť a zistiť, či sa vrátia charakteristické príznaky FIP. Mačka bola nakoniec eutanizovaná a pri pitve bolo zistené, že má vrodený typ HCM a žiadne zvyškové lézie FIP alebo vírusovej RNA v akýchkoľvek tkanivách. Dilatačná kardiomyopatia bola hlásená u 17,6% ľudí infikovaných HIV pri chronickej antiretrovírusovej liečbe. Dospelo sa však k záveru, že príčinou srdcového ochorenia u tejto mačky nebol GS441524. Ochorenie srdca u tejto mačky bolo hypertrofické na rozdiel od dilatačnej formy pozorovanej u pacientov s HIV, a navyše je HCM u útulkových mačiek pomerne bežná.
Závery
Výsledky získané od 31 mačiek liečených GS-441524 prekonali všetky očakávania a naznačujú, že FIP, bez ohľadu na signalizáciu alebo formu ochorenia, je s použitím nukleozidových analógov liečiteľné ochorenie. Koncepcia štúdie a parametre liečby vyplývajúce z tohto obmedzeného klinického testovania budú dôležité pre ďalšie úsilie v komercializácii tohto alebo podobných liekov proti FIP.
Doplnkový materiál



Poďakovania
Ďakujeme pracovníkom Centra pre zdravie spoločenských zvierat za pomoc pri preprave liekov (Lyra Pineda-Nelson a Nancy Bei) a za prezentáciu údajov (Cynthia Echeverria). Sme vďační najmä mnohým majiteľom a 31 mačkám, ktoré sa zúčastnili emotívnej a náročnej cesty, ktorá predčila všetky očakávania. Sme vďační aj praktickým súkromným veterinárom, ktorí pomáhali s pravidelnými krvnými testami a boli tu pre nás a ich pacientov/majiteľov, keď to bolo potrebné.
Poznámky
Prijaté: 28. decembra 2018
Doplnkový materiál: K dispozícii sú nasledujúce súbory: Formulár súhlasu klienta.
Obrázok S1: Priemerné hladiny pečeňových enzýmov (IU / l) u mačiek počas liečby GS-441524. Počas celých liečebných období sa nepozorovali žiadne významné zmeny.
Obrázok S2: Priemerné hladiny lipázy a amylázy v sére (IU / l) u mačiek počas liečby GS-441524. Počas celých liečebných období sa nepozorovali žiadne významné zmeny.
Obrázok S3: Priemerné hladiny urey a kreatinínu v krvi u mačiek počas liečby GS-441524. Počas celých liečebných období sa nepozorovali žiadne významné zmeny.
Konflikt záujmov: MP a EM sú zamestnancami spoločnosti Gilead Sciences, Foster City, CA, USA a majú v spoločnosti podiely.
Finančné prostriedky: Finančnú podporu pre túto štúdiu poskytli Centrum pre spoločenské zdravie zvierat UC Davis, Fond Philipa Raskina v Kansas City a početní darcovia organizácii SOCK FIP podľa pokynov pani Carol Horace. GS-441524 použitý v tomto pokuse bol poskytnutý spoločnosťou Gilead Sciences, Foster City, CA.
Literatúra
| 1. | De Clercq, E, Li, G. Approved antiviral drugs over the past 50 years. Clin Microbiol Rev 2016; 29: 695–747. Google Scholar | Crossref | Medline |
| 2. | Hartmann, K. Efficacy of antiviral chemotherapy for retrovirus-infected cats: what does the current literature tell us? J Feline Med Surg 2015; 17: 925–939. Google Scholar | SAGE Journals | ISI |
| 3. | Thomasy, SM, Shull, O, Outerbridge, CA. Oral administration of famciclovir for treatment of spontaneous ocular, respiratory, or dermatologic disease attributed to feline herpesvirus type 1: 59 cases (2006–2013). J Am Vet Med Assoc 2016; 249: 526–538. Google Scholar | Crossref | Medline |
| 4. | Pedersen, NC, Elliott, JB, Glasgow, A. An isolated epizootic of hemorrhagic-like fever in cats caused by a novel and highly virulent strain of feline calicivirus. Vet Microbiol 2000; 73: 281–300. Google Scholar | Crossref | Medline | ISI |
| 5. | Kim, Y, Shivanna, V, Narayanan, S. Broad-spectrum inhibitors against 3C-like proteases of feline coronaviruses and feline caliciviruses. J Virol 2015; 89: 4942–4950. Google Scholar | Crossref | Medline |
| 6. | Pedersen, NC, Kim, Y, Liu, H. Efficacy of a 3C-like protease inhibitor in treating various forms of acquired feline infectious peritonitis. J Feline Med Surg 2018; 20: 378–392. Google Scholar | SAGE Journals | ISI |
| 7. | Pesteanu-Somogyi, LD, Radzai, C, Pressler, BM. Prevalence of feline infectious peritonitis in specific cat breeds. J Feline Med Surg 2006; 8: 1–5. Google Scholar | SAGE Journals | ISI |
| 8. | Riemer, F, Kuehner, KA, Ritz, S. Clinical and laboratory features of cats with feline infectious peritonitis – a retrospective study of 231 confirmed cases (2000–2010). J Feline Med Surg 2016; 18: 348–356. Google Scholar | SAGE Journals | ISI |
| 9. | Rohrbach, BW, Legendre, AM, Baldwin, CA. Epidemiology of feline infectious peritonitis among cats examined at veterinary medical teaching hospitals. J Am Vet Med Assoc 2001; 218: 1111–1115. Google Scholar | Crossref | Medline | ISI |
| 10. | Warren, TK, Jordan, R, Lo, MK. Therapeutic efficacy of the small molecule GS-5734 against Ebola virus in rhesus monkeys. Nature 2016; 531: 381–385. Google Scholar | Crossref | Medline | ISI |
| 11. | Sheahan, TP, Sims, AC, Graham, RL. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses. Sci Transl Med 2017; 9. DOI: 10.1126/scitranslmed.aal3653. Google Scholar | Crossref |
| 12. | Murphy, BG, Perron, M, Murakami, E. The nucleoside analog GS-441524 strongly inhibits feline infectious peritonitis (FIP) virus in tissue culture and experimental cat infection studies. Vet Microbiol 2018; 219: 226–233. Google Scholar | Crossref | Medline |
| 13. | Takano, T, Endoh, M, Fukatsu, H. The cholesterol transport inhibitor U18666A inhibits type I feline coronavirus infection. Antiviral Res 2017; 145: 96–102. Google Scholar | Crossref | Medline |
| 14. | Takano, T, Nakano, K, Doki, T. Differential effects of viroporin inhibitors against feline infectious peritonitis virus serotypes I and II. Arch Virol 2015; 160: 1163–1170. Google Scholar | Crossref | Medline |
| 15. | Kim, Y, Liu, H, Galasiti Kankanamalage, AC. Reversal of the progression of fatal coronavirus infection in cats by a broad- spectrum coronavirus protease inhibitor. PLoS Pathog 2016; 12: DOI: 10.1371/journal.ppat.1005531. Google Scholar | Crossref |
| 16. | Gut, M, Leutenegger, CM, Huder, JB. One-tube fluorogenic reverse transcription-polymerase chain reaction for the quantitation of feline coronaviruses. J Virol Methods 1999; 77: 37–46. Google Scholar | Crossref | Medline | ISI |
| 17. | Agostini, ML, Andres, EL, Sims, AC. Coronavirus susceptibility to the antiviral remdesivir (GS-5734) is mediated by the viral polymerase and the proofreading exoribonuclease. MBio 2018; 9. DOI: 10.1128/mBio.00221-18. Google Scholar |
| 18. | Weiss, G, Goodnough, LT. Anemia of chronic disease. N Engl J Med 2005; 352: 1011–1023. Google Scholar | Crossref | Medline | ISI |
| 19. | Kurnick, JE, Ward, HP, Pickett, JC. Mechanism of the anemia of chronic disorders: correlation of hematocrit value with albumin, vitamin B12, transferrin, and iron stores. Arch Intern Med 1972; 130: 323–326. Google Scholar | Crossref | Medline |
| 20. | Taylor, SS, Tappin, SW, Dodkin, SJ. Serum protein electrophoresis in 155 cats. J Feline Med Surg 2010; 12: 643–653. Google Scholar | SAGE Journals | ISI |
| 21. | Hirschberger, J, Hartmann, K, Wilhelm, N. Clinical symptoms and diagnosis of feline infectious peritonitis. Tierarztl Prax 1995; 23: 92–99. Google Scholar | Medline |
| 22. | Pedersen, NC, Liu, H, Gandolfi, B. The influence of age and genetics on natural resistance to experimentally induced feline infectious peritonitis. Vet Immunol Immunopathol 2014; 28: 152–154. Google Scholar |
| 23. | Jain, N, Reddy, DH, Verma, SP. Cardiac abnormalities in HIV-positive patients: results from an observational study in India. J Int Assoc Provid AIDS Care 2014; 13: 40–46. Google Scholar | SAGE Journals |
| 24. | Payne, JR, Brodbelt, DC, Luis Fuentes, V. Cardiomyopathy prevalence in 780 apparently healthy cats in rehoming centres (the CatScan study). J Vet Cardiol 2015; 17 Suppl 1: S244–S257. Google Scholar | Crossref | Medline |