Pôvodný článok: Efficacy of a 3C-like protease inhibitor in treating various forms of acquired feline infectious peritonitis
Publikovaný: 13.9.2017, SAGE – Journal of Feline Medicine and Surgery
Niels C Pedersen,1 Yunjeong Kim,2 Hongwei Liu,1 Anushka C Galasiti Kankanamalage,3 Chrissy Eckstrand,4 William C Groutas,3 Michael Bannasch,1 Juliana M Meadows,5 and Kyeong-Ok Chang2
Abstrakt
Cieľ
Bezpečnosť a účinnosť inhibítora 3C-Like proteázy GC376 bola testovaná na skupine klientmi vlastnených mačiek s rôznymi formami infekčnej peritonitídy (FIP).
Metódy
Do klinického testu bolo prijatých 20 mačiek vo veku od 3,3 do 82 mesiacov (priemerne 10,4 mesiaca) s rôznymi formami FIP. Štrnásť mačiek malo vlhkú alebo zmiešanú FIP a šesť mačiek malo suchú FIP. GC376 sa podával subkutánne každých 12 hodín v dávke 15 mg/kg. Mačky s neurologickými príznakmi boli zo štúdie vylúčené.
Výsledky
Devätnásť z 20 mačiek liečených GC376 sa uzdravilo do 2 týždňov od začiatku liečby. Príznaky choroby sa však po 1–7 týždňoch od primárnej liečby vrátili, a relapsy a nové prípady sa nakoniec liečili minimálne 12 týždňov. Relapsy, ktoré prestali reagovať na liečbu, sa vyskytli u 13 z týchto 19 mačiek v priebehu 1-7 týždňov od počiatočnej alebo opakovanej liečby. Závažné neurologické ochorenie sa vyskytlo u 8/13 mačiek, u ktorých zlyhala liečba, a u piatich mačiek sa opakovali brušné lézie. V čase písania tohto článku bolo sedem mačiek v remisii choroby. Päť mačiatok vo veku 3,3–4,4 mesiaca s vlhkou FIP bolo liečených 12 týždňov a po ukončení liečby a v čase písania článku boli v remisii ochorenia 5–14 mesiacov (priemerne 11,2 mesiaca). Šieste mačiatko bolo po 12 týždňoch liečby v remisii 10 týždňov, došlo však k relapsu a dobre reaguje na druhé kolo liečby s GC376. Siedma bola 6,8-ročná mačka s postihnutím mezenterických lymfatických uzlín, ktorej sa podarilo dosiahnuť remisiu po troch relapsoch, ktoré si vyžadovali postupne dlhšie opakované liečby počas 10 mesiacov. Vedľajšie účinky liečby zahŕňali pálenie pri aplikácii injekcie a občasné ložiská subkutánnej fibrózy a vypadávanie chlpov. U mačiek liečených pred 16.-18. týždňom došlo k spomalenému vývoju a abnormálnemu rastu trvalých zubov.
Závery a význam
GC376 sa ukázal byť sľubný pri liečbe mačiek s konkrétnymi formami FIP a otvoril tak dvere k cielenej antivírusovej liečbe.
Úvod
Lieky, ktoré priamo inhibujú replikáciu vírusov, sa stali kľúčovými oporami pri liečbe chronických vírusových infekcií, ako je HIV/AIDS, vírusu hepatitídy C (HCV), vírusu hepatitídy B, herpesvírusu a akútnych infekcií, ako je chrípka. RNA vírusy, ako sú HIV-1 a HCV, obsahujú ideálne ciele pre inhibíciu vírusov, ako sú RNA-závislá RNA polymeráza a proteáza. Proteázy sú obzvlášť dobrým cieľom, pretože sa podieľajú na dozrievaní vírusov (HIV) alebo na produkcii funkčných vírusových proteínov (HCV). Inhibítory proteázy sa tiež používajú v kombinácii s inhibítormi reverznej transkripcie pri celoživotnej liečbe HIV/AIDS. Kombinácie rôznych inhibítorov proteázy sú vysoko účinné pri liečbe infekcie HCV u ľudí. Preto nie je prekvapujúce, že vírusová proteáza by mala byť atraktívny cieľ aj pre výskum infekcií zvierat spôsobených RNA vírusom. Kim a kol. syntetizovali peptidylové zlúčeniny, ktoré sú zamerané na 3C-like (3CLpro) proteázy, a hodnotila ich účinnosť proti mačaciemu koronavírusu (FCoV) a mačaciemu kalicivírusu, ako aj proti dôležitým ľudským RNA vírusom, ktoré kódujú 3CLpro alebo príbuznú 3C proteázu. Identifikovali sériu zlúčenín, ktoré vykazovali silnú inhibičnú aktivitu proti rôznym koronavírusom, vrátane FCoV, s vysokým rozsahom bezpečnosti. Účinnosť ich inhibítorov 3CLpro bola predmetom pokusov u myší infikovaných vírusom hepatitídy A59, myšacím koronavírusom, a zistilo sa, že spôsobujú významné zníženie titrov vírusov a patologických lézií.
V súčasnosti neexistujú komerčne dostupné antivírusové lieky na koronavírusové infekcie u ľudí alebo zvierat a štúdie Kim a kol. dokázali, že inhibícia 3CLpro môže viesť k potlačeniu replikácie koronavírusu in vivo. Ukázali, že niektoré z ich inhibítorov 3CLpro sú vhodné ako terapeutické prostriedky proti týmto dôležitým vírusom u domácich a divokých mačiek. Potvrdila to štúdia s využitím experimentálnej infekcie vírusom mačacej infekčnej peritonitídy u laboratórnych mačiek. Aj keď je experimentálna infekcia FIPV vysoko smrteľná, akonáhle infekcia dosiahla definovateľné štádium, 14–20 dní trvajúca liečba pomocou GC376 viedla k rýchlej remisii ochorenia u šiestich mačiek, ktorá v čase publikácie článku trvala už viac ako 12 mesiacov.
Materiály a metódy
Oficiálne protokoly
Táto štúdia prebiehala podľa protokolu 18731 schváleného Inštitucionálnym výborom pre starostlivosť a použitie zvierat a Výborom pre hodnotenie klinických skúšok Komisie pre klinické skúšky veterinárnej lekárskej fakultnej nemocnice na Kalifornskej univerzite v Davise. Tento protokol podrobne popisuje podmienky testovania nového inhibítora proteázy GC376 u mačiek vlastnených klientom. Každý vlastník bol povinný prečítať si podmienky štúdie a vyjadriť s nimi súhlas.
Organizácia klinickej štúdie
Predmetom štúdie bolo vyhodnotenie inhibítora 3CLpro GC376 u skupiny mačiek s prirodzene získanou FIP. Štúdia nezahŕňala skupinu s placebom, pretože, ako poznamenali Miller a Brody, „hlavnou etickou zásadou v placebom kontrolovaných klinických skúškach je, že pokiaľ pre daný stav existuje preukázaná účinná liečba, je testovanie proti placebu neetické“. GC376 sa už preukázal ako vysoko účinný pri liečbe mačiek s experimentálne indukovanou FIP pred touto štúdiou, čím vznikol predpoklad existujúcej účinnej liečby. Placebo kontrolu nahradila skupina s prirodzene prebiehajucou chorobou. Žiadna z 20 liečených mačiek nepreukázala pretrvávajúce priaznivé reakcie na liečbu, ktorú dostali pred liečbou GC376.
Inštitucionálne pravidlá vylúčili použitie mačiek získaných z útulkov alebo podobných zariadení na výskum tohto typu, a vyžadovali, aby všetky mačky boli v legálnom vlastníctve/adoptované, a aby sa s nimi zaobchádzalo s výslovným súhlasom majiteľa. Mačky s klinicky zjavným neurologickým ochorením boli vylúčené. Do štúdie bolo nakoniec zahrnutých 20 mačiek z rôznych oblastí USA, rôzneho veku a s rôznymi formami FIP. Táto relatívne malá skupina mačiek poskytla cenné poznatky o koncepcii pokusu, interakcii a súlade s vlastníkom, sledovaní bezpečnosti a účinnosti, stanovení minimálneho dávkovacieho režimu, hodnotení relapsov choroby počas liečby alebo po nej a stanovení klinických foriem FIP, ktoré sú pre liečbu najvhodnejšie. Tieto informácie, dúfajme, pomôžu pri ďalších testoch potrebných na udeľovanie licencií a prípadnú komercializáciu GC376 a na vykonávanie podobných testov budúcich antivírusových liekov na FIPV a iných chronických vírusových infekcií mačiek.
Popis testovacej skupiny
Do pokusu bolo zapojených 20 mačiek a ich majiteľov a príslušné informácie o každej mačke sú uvedené v tabuľke 1 a o celej pokusnej skupine na obrázku 1. Mačky boli do štúdie zaradené s rôznym stupňom predbežného testovania zo strany veterinárnych lekárov primárnej starostlivosti. Toto testovanie zvyčajne zahŕňalo kompletný krvný obraz (CBC) s celkovým plazmatickým proteínom, globulínom (G), albumínom (A), A:G; chemický profil séra a analýzu výpotkov vrátane celkového proteínu, skutočného alebo odhadovaného počtu buniek a typu zápalových buniek. U malého podielu mačiek sa uskutočnilo ďalšie testovanie, ktoré obsahovalo titre protilátok FIPV, ultrazvuk brušnej alebo hrudnej oblasti, biopsie postihnutého tkaniva a kvantitatívnu PCR v reálnom čase (qRT-PCR) z výpotkov.
Tabuľka 1
Základné údaje, pôvod, hlavné klinické príznaky a hlavné zistenia pri pitve po liečbe inhibítorom proteázy GC376
| ID/Meno | Vek (mes.) | Hmotnosť (kg) | Pohlavie | Plemeno | Pôvod | Symptómy | Stav | Pitva |
|---|---|---|---|---|---|---|---|---|
| CT01 (Echo) | 5.6 | 1.64 | FS | DSH | KR | Peritonitída, zakrpatená | – | B, Int |
| CT02 (Cate) | 6 | 2.67 | FS | DLH | KR | Peritonitída, zakrpatená | – | B, E, Int, L, MLN |
| CT03 (Pancake) | 7.86 | 3.18 | MC | Him | CT | Suchá (Col) až vlhká | + | Int, L, MLN, S, Om, P |
| CT04 (Kratos) | 82 | 4.8 | MC | DSH | KR | Suchá (MLN) | Remisia | |
| CT05 (Scooter) | 10 | 4.25 | MC | DSH | KR | Suchá (E, MLN, K) | – | B, E, L, K, MLN |
| CT07 (Mac) | 6.6 | 2.6 | MC | DSH | KR | Suchá (Col) | + | E, Int, L, MLN, S, K, A, Lu |
| CT08 (Phoebe) | 4.2 | 2.18 | FS | DSH | KR | Suchá (E) | – | B, E, K, MLN, S |
| CT09 (Sammy) | 10.5 | 2.89 | MC | DSH | KR | Suchá (MLN, K) | ?* | B* |
| CT10 (Bandit) | 17.9 | 4.06 | MC | Him | CT | Suchá (Col) až vlhká | + | B, E, Int, L, MLN, K, Om, P, Lu |
| CT12 (Daisy) | 7.5 | 2.5 | FS | DSH | KR | Peritonitída, zakrpatená | – | B, Int, L, S |
| CT13 (Leo) | 7.4 | 1.97 | MC | Sphynx | CT | Suchá (E, K) | + | B, E, Int, L, MLN, S, K |
| CT14 (Muffin) | 8 | 2.94 | FS | DSH | KR | Suchá (Col) až vlhká | + | E, Int, L, MLN, K, Om, P |
| CT15 (Flora) | 4.3 | 2.39 | F | DSH | FC | Peritonitída | Remisia | |
| CT16 (Bean) | 4 | 1.4 | FS | DSH | KR | Peritonitída, zakrpatená | + | B,† E, Int, L, MLN, S, Om, P |
| CT17 (Peanut) | 4.4 | 2.3 | M | DSH | KR | Peritonitída | Remisia | |
| CT18 (Smokey) | 4 | 1.84 | MC | DSH | KR | Peritonitída | Remisia | |
| CT20 (Cloud) | 3.3 | 1.55 | M | RM | CT | Pleuritída (MLN) | Remisia | |
| CT21 (Phoebe) | 4.8 | 1.92 | F | DSH | KR | Peritonitída | Remisia/relaps/opakovaná liečba | |
| CT22 (Pepper) | 3.3 | 1.6 | F | Sibírska | CT | Peritonitída | + | B, E, Om, MLN, Lu, Dia |
| CT23 (Oakely) | 3.9 | 3.1 | FS | DSH | KR | Peritonitída | Remisia | |
| Priemer | 10.28 | 2.59 | ||||||
| SD | 17.22 | 0.94 |
*Neuskutočnila sa žiadna pitva, ale boli prítomné terminálne neurologické príznaky
† Ťažký mozgový edém, neboli zaznamenané žiadne typické zápalové lézie

Demografické údaje o mačkách zaradených do štúdie. (a–c) Koláčové grafy sumarizujúce percento pacientov: (a) vek v mesiacoch, (b) plemeno alebo (c) pôvod. (d) Stĺpcový graf zobrazujúci formy mačacej infekčnej peritonitídy (FIP) zaradených pacientov.
M = mesiace; DSH = domáca krátkosrstá; DLH = domáca dlhosrstá; MD = Maryland; OH = Ohio; Tx = Texas; FL = Florida; IL = Illinois; CT = Connecticut; CA = Kalifornia
Mačky s klinickými príznakmi svedčiacimi o neurologickom postihnutí boli zo štúdie vylúčené na základe skorších nepublikovaných experimentálnych štúdií s GC376. Jedna mačka, ktorá dlhodobo prežila predchádzajúcu štúdiu farmakokinetiky a účinnosti GC376, mala recidívu FIP prejavujúcu sa neurologickými príznakmi 6 mesiacov po tom, čo sa javila ako úspešná liečba akútnej infekcie.6 Táto mačka nereagovala na opakovanú procedúru s GC376, ktorá podnietila štúdiu schopnosti lieku preniknúť do mozgu. Úrovne GC376 v mozgu laboratórnych mačiek predstavovali iba 3% plazmatických koncentrácií liečiva.
Potvrdenie ochorenia
Diagnóza FIP bola potvrdená v čase vstupu do štúdie na základe základných údajov, klinickej anamnézy, vyšetrenia výsledkov predchádzajúcich laboratórnych testov, fyzikálneho vyšetrenia a opakovania základných analýz krvi a výpotku. Ručná palpácia brucha bola zvyčajne dostatočná na identifikáciu ascitu, zväčšených mezenterických lymfatických uzlín, zväčšenia slepého čreva a s nimi spojených ileo-cekálno-kolických lymfatických uzlín, tumorov v obličkách a infiltrácie hrubého čreva. Ručná palpácia sa v prípade potreby doplnila ultrazvukom. Oči sa spočiatku vyšetrovali priamym svetlom na akékoľvek abnormality v sietnici, na zrazeniny v prednej komore alebo na zadnej strane rohovky a záblesky v komorovej vode. Prítomnosť očného ochorenia sa potvrdila úplným oftalmoskopickým vyšetrením vykonaným oftalmologickou službou Veterinárnej lekárskej fakultnej nemocnice (VMTH), UC Davis. Prítomnosť FIPV sa ďalej potvrdila pomocou qRT-PCR, buď z brušných alebo hrudných výpotkov odobratých v čase prijatia, alebo v čase pitvy. Sekvenovanie génu FIPV proteázy sa uskutočňovalo na mačkách, u ktorých došlo k relapsu počas liečby, aby sa určilo, či došlo k potenciálnej mutácii spôsobujúcej rezistenciu na liečivo.
Diagnóza FIP sucho-vlhkej (zmiešanej) FIP u troch mačiek (CT03, CT10 a CT14) bola založená na difúznom zväčšení hrubého čreva a anamnéze riedkej stolice, krvi a hlienu v stolici, napínania na defekáciu a stolice malého kalibru pred výskytom brušných efúzií. FIP hrubého čreva bola opísaná ako špecifická variantná forma neefuzívnej FIP. Podozrenie na zmiešanú FIP bolo aj u mačiek CT01, CT02 a CT12 z dôvodu zastavenia rastu, ktorý o mnoho týždňov predchádzal výskyt brušných výpotkov.
Liečebný režim
GC376 bol syntetizovaný vo vysoko čistej forme a pripravený v koncentrácii 53 mg/ml v 10% etanole a 90% polyetylénglykole 400, ako bolo opísané vyššie. GC376 bol podávaný subkutánne (SC) v dávke 15 mg/kg každých 12 hodín SC, pokiaľ nie je uvedené inak. Účinná dávka pre mačky s experimentálne indukovanou FIP bola 10 mg/kg / q12 h SC, ale dávka sa zvýšila na 15 mg/kg potom, čo prvá mačka (CT01) nereagovala na nižšiu dávku 10 mg/kg stanovenú predchádzajúcimi farmakokinetickými štúdiami. Išlo o klinické rozhodnutie založené na reakcii tejto jednej mačky na liečbu.
Monitorovanie odpovede na liečbu
Mačky s FIP boli na základe predbežného testovania a počiatočného vyhodnotenia v čase prezentácie na UC Davis hospitalizované najmenej 5 dní a okamžite začali liečbu. Najmenej dvakrát denne boli podrobne vyšetrené na rektálnu teplotu, pulz, dýchanie, chuť do jedla a aktivitu. Použila sa hrudkujúca podstielka, ktorá umožňovala denné hodnotenie objemu a konzistencie stolice a močenia. Celá krv sa odoberala do EDTA alebo heparínu venepunkciou pred zahájením liečby, v dvojdňových intervaloch počas hospitalizácie, v čase prepustenia a v dvojtýždňových intervaloch počas prvého mesiaca a potom v mesačných alebo väčších intervaloch. Rutinné vyšetrenie krvi v každom časovom bode zahŕňalo minimálne hematokrit, celkový plazmatický proteín, ikterický index, celkový počet bielych krviniek, diferenciálny rozpočet bielych krviniek a absolútny počet neutrofilov, lymfocytov a monocytov a eozinofilov. Kvôli kontrole potenciálnej toxicity liekov sa pravidelne zaznamenávali hodnoty chemického zloženia krvného séra. Vzorky brušných výpotkov sa získavali paracentézou každý druhý deň, pokiaľ sa dali získať, čo bolo zvyčajne prvých 3–7 dní. Mačky s dýchavičnosťou boli vyšetrené hrudnou ultrasonografiou a vzorka tekutín bola získaná ultrazvukom vedenou paracentézou. Výpotky sa skúmali na prítomnosť fibrínových zrazenín, prímes neutrofilov a malých/veľkých mononukleárnych buniek, intenzitu žltého sfarbenia, viskozitu pôsobením vlákien a celkový obsah bielkovín. Bunkové pelety z peritoneálnych alebo hrudných výpotkov boli tiež skúmané pomocou qRT-PCR na hladinu vírusovej RNA, ako už bolo opísané.
Mačky boli vydané svojim majiteľom, keď bola zaznamenaná pozitívna reakcia na liečbu, zvyčajne do 5 dní. Majiteľ (majitelia) boli buď vedúcim veterinárnym lekárom, alebo veterinárnym lekárom primárnej starostlivosti poučení, ako podať liek dvakrát denne subkutánnou injekciou. Miesta vpichu sa menili tak, aby zahŕňali hornú líniu od zátylku po strednú časť chrbta a po stranách hrudníka a bokov. Dbalo sa na to, aby sa zabránilo ukladaniu liečiva do dermis alebo postupne na rovnakom podkožnom mieste. Majitelia boli vyzvaní, aby udržiavali denné záznamy o rektálnej teplote, aktivite, chuti do jedla, defekácii a močení a týždenné až dvojtýždňové telesné hmotnosti. Periodické vzorky krvi pre CBC a chemické hodnoty séra boli odoberané osobnými veterinárnymi lekármi majiteľov a zaslané do komerčných veterinárnych diagnostických laboratórií. Akékoľvek abnormálne príznaky alebo správanie bolo potrebné zaznamenať a okamžite hlásiť. Eutanázia sa v prípade potreby uskutočňovala buď na UC Davis, alebo veterinárnym lekárom primárnej starostlivosti. Telá mačiek usmrtené veterinárnymi lekármi primárnej starostlivosti boli okamžite schladené a odoslané v obaloch s ľadom expresnou poštou do UC Davis na pitvu. Požiadavky majiteľov o zaobchádzanie a konečnú dispozíciu tela boli rešpektované.
Výsledky
Stanovenie dĺžky liečby
Prvých päť mačiek v štúdii bolo spočiatku liečených 2 týždne (CT01, CT02, CT03, CT04 a CT05). U všetkých mačiek bolo pozorované rýchle zlepšenie zdravotného stavu a liečba bola ukončená. Napriek priaznivej počiatočnej odpovedi sa príznaky ochorenia opakovali 1 (CT01, CT05), 2 (CT03, CT04) alebo 7 (CT02) týždňov po ukončení 2-týždňovej liečby (obrázok 2). Mačky boli potom liečené znova, dôvodom bolo postupné predlžovanie primárnej a sekundárnej doby liečby, kým ich FIP ostávala citlivá na GC376 (pozri CT04, CT22, obrázok 2). Nové mačky, ktoré sa dostali do štúdie, sa ďalej liečili 3 (CT07) alebo 4 týždne (CT08, CT16). Mačky CT08 a CT16 spočiatku reagovali, ale ich príznaky choroby sa počas liečby objavili znova. U mačky CT08 sa vyvinula neurologická choroba, zatiaľ čo u mačky CT16 sa opakovane vyskytli brušné lézie (tabuľka 1). Primárne a sekundárne liečebné doby sa potom predĺžili na 9 týždňov (CT07, CT09, CT10, CT14) (obrázok 2). U mačky CT09 sa vyvinuli neurologické príznaky počas 9-týždňovej základnej liečby a nakoniec bola utratená, keď sa príznaky choroby stali závažnými. U mačky CT07 sa vyskytlo neurologické ochorenie 6 týždňov po začiatku druhej liečby. Od tohto bodu boli všetky nové mačky prijaté to štúdie a staršie mačky, ako napríklad CT10, liečené alebo znovu liečené najmenej 12 týždňov. Prínos 12-týždňovej liečby bol najzrejmejší u mačky CT04, ktorá bola predtým liečená už trikrát s kratšou dobou liečby nasledovanou relapsom (obrázok 2). Liečba bola ukončená u mačiek, ktoré nemali klinické ani laboratórne príznaky choroby po 12 týždňoch primárnej ani sekundárnej liečby. Zistilo sa, že minimálna doba liečby by mala byť okolo 12 týždňov. Mačka CT21 bola liečená 17 týždňov z dôvodu oneskoreného zlepšenia počtu celkových bielkovín a bielych krviniek (obrázok 2). U tejto mačky došlo k relapsu pleurálnej FIP o 13 týždňov neskôr a v čase písania tohto článku bola podrobená ďalšej liečbe.

Časová škála liečby a klinický výsledok 20 mačiek, ktoré vstúpili do klinickej štúdie s inhibítorom proteázy GC376. Obdobia, počas ktorých boli mačky liečené, sú označené plnými čiarami. Je uvedený dátum posledného dňa liečby pre šesť mačiek, ktoré dosiahli trvalú klinickú remisiu. Mačka 21 bola v čase písania tohto článku ešte v liečbe. Zvyšných 13 mačiek podľahlo neneurologickej FIP alebo neurologickej FIP po ukončení primárnej alebo sekundárnej liečby do 0-7 týždňov
Odpoveď na počiatočnú liečbu a ukazovatele priaznivej reakcie
Počas prvých 1–4 týždňov liečby sa u 19/20 mačiek prejavilo dramatické a progresívne zlepšovanie zdravotného stavu. Výnimkou bola mačka CT16, ktorá reagovala poklesom teploty v konečníku počas prvých 4 dní liečby. Horúčka sa však vrátila a zdravotný stav sa nasledujúcich 23 dní naďalej zhoršoval a mačka bola eutanizovaná. Horúčka (>38,9 °C) u ďalších 19 mačiek zmizla do 24–48 hodín, so súčasným zlepšením chuti do jedla, aktivity, rastu a prírastku hmotnosti. Brušné výpotky boli zvyčajne nezistiteľné do 2 týždňov. Zvyškový hrudný výpotok zostávajúci po počiatočnej terapeutickej drenáži po 3 dňoch u mačky CT20 takmer zmizol. Renálne tumory u mačiek CT02 a CT13 sa tiež rýchlo zmenšili a po 2 týždňoch už neboli hmatateľné. Zväčšené mezenterické lymfatické uzliny sa k normálnej veľkosti vracali pomalšie. Hmatateľné zhrubnutie hrubého čreva a s ním spojené ileo-cekálno-kolické útvary reagovali najpomalšie a u mačky CT03 pretrvávali aj napriek liečbe a návratu k inak normálnemu zdravotnému stavu. Žltačka, častý nález u mladších mačiek s efuzívnou FIP, pomaly ustupovala počas 2 alebo viac týždňov, súčasne so znižovaním hyperbilirubinémie. Príznaky očnej choroby začali miznút do 48 hodín a zmizli do 1 týždňa bez ohľadu na počiatočnú závažnosť (obrázok 3).

Vzhľad očí mačky CT08 pred zahájením liečby (a) a o týždeň neskôr (b). U tejto mačky sa o 3 týždne po začiatku liečby rozvinuli závažné neurologické príznaky.
Prírastok hmotnosti bol jednoduchým a presným kritériom rastu a zlepšenia zdravia. Ako vzťažná hodnota pre tento parameter bola použitá hmotnosť mačky CT04, najstaršej mačky v teste (obrázok 4a). Mačka CT04 vykazovala signifikantný úbytok hmotnosti o 30%. Po každom kole liečby pribrala, krátko pred každým relapsom choroby začala chudnúť a po každej liečbe opäť pribrala. Po 9,3 mesiacoch bez liečby a po liečbe (4,8 kg až 7,19 kg) znovu získala všetku svoju stratenú váhu. Všetky mačiatka s trvalou remisiou počas a po antivírusovej liečbe ustavične priberali na váhe, čo naznačuje, že pri antivírusovej liečbe pokračoval normálny rast (obrázok 4b). Jedna mačka (CT15) a dvaja kocúri (CT17, 20) boli bez komplikácií kastrovaní počas remisie choroby.

Antivírusová liečba a zmeny telesnej hmotnosti. (a) Mačka CT04, 6,8-ročný kastrovaný samec, ktorý mal suchú mačaciu infekčnú peritonitídu (FIP), absolvoval štyri cykly antivírusovej liečby s narastajúcim trvaním, ako je znázornené bodkovanými políčkami. Pred každou recidívou schudol a po následnej liečbe pribral. (b) Prírastky hmotnosti u štyroch mačiatok vo veku 3,5-4,4 mesiaca počas a po antivírusovej liečbe sú znázornené bodkami. Bodkovaný obdĺžnik označuje dĺžku antivírusovej liečby (12 týždňov)
Lymfopénia bola bežným klinickým príznakom mačiek s vlhkou FIP (obrázok 5) a mala tendenciu priamo korelovať so závažnosťou brušného zápalu, čo naznačovala viskozita, prítomnosť fibrínových vlákien, obsah bielkovín, počet buniek a stupeň žltej farby výpotku. Lymfopénia sa zlepšila pri liečbe všetkých mačiek s vlhkou FIP okrem CT16, ale nepomohla predpovedať relapsy choroby, ktoré sa vyskytli potom (obrázok 5a). U mačiek so suchou FIP lymfopénia nebola tak výrazná, a pre hodnotenie odpovede na liečbu nebola užitočná tak, ako iné parametre (obrázok 5b).

Priemer a smerodajná odchýlka (SD) absolútneho počtu lymfocytov u liečených pacientov s (a) vlhkou alebo (b) suchou mačacou infekčnou peritonitídou (FIP). a) Dvanásť mačiek (prázdny krúžok), u ktorých sa prejavil brušný alebo hrudný výpotok, a ktoré boli liečené až 12 týždňov. Trinásta mačka (CT16, plný krúžok) s brušným výpotkom reagovala na liečbu zle. b) Sedem mačiek so suchou alebo vlhkou formou FIP a s následnou liečbou v trvaní 6 týždňov.
Celkové hladiny bielkovín v plazme ako nepriamy indikátor koncentrácie globulínu boli pri vyšetrení často zvýšené, ale hodnoty boli počas prvých 4 týždňov veľmi variabilné a často prechodne stúpali počas resorpcie výpotkov. Mačky, u ktorých nakoniec liečba nebola úspešná, mali tendenciu mať vyššie celkové koncentrácie plazmatických proteínov na začiatku liečby a mali tendenciu udržiavať si vyššie hladiny počas liečby ako mačky, ktoré úspešne dosiahli trvalú remisiu (obrázok 6).
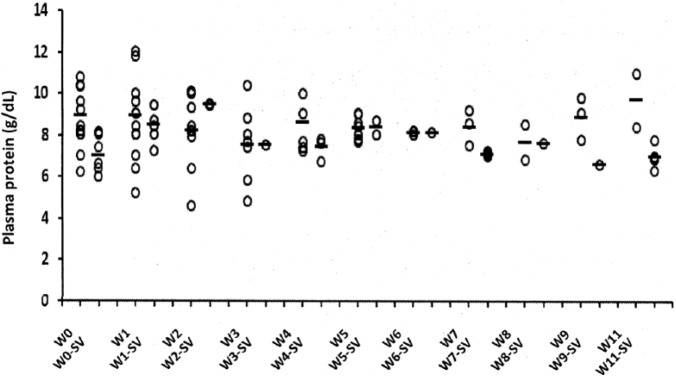
Priemer a SD celkových hladín bielkovín v plazme u 20 mačiek počas obdobia 12 týždňov. Trinásť mačiek utrpelo v rôznych týždňoch liečby (W) smrteľné relapsy a sedem mačiek dosiahlo trvalú remisiu po 12 týždňoch liečby (W-SV)
Zníženie hladiny vírusovej RNA v bunkách z ascitickej tekutiny v spojitosti s liečbou
Sekvenčné vzorky ascitu boli odobraté niekoľkým tým istým mačkám počas prvých 6–25 dní antivírusovej liečby a boli testované na hladiny vírusovej RNA pomocou qRT-PCR. Hladiny FIPV sú často nízke alebo negatívne v krvi mačiek s FIP a najvyššie sú v bunkách z výpotkov. Preto boli najspoľahlivejším zdrojom FIPV RNA bunky z ascitu alebo pleurálneho výpotku. Mačky CT15, CT16 a CT17 mali 955, 1699 a 2937-krát vyššie hladiny vírusovej RNA, v danom poradí, ako CT02, ktoré mali najnižšiu vírusovú záťaž v efúzii pred liečbou (obrázok 7). Hladiny vírusovej RNA sa v priebehu 2 týždňov znížili až 1567463-násobne v porovnaní s hodnotami pred liečbou, s výnimkou mačky CT16 (obrázok 8), ktorá mala druhú najvyššiu hladinu vírusovej RNA pred antivírusovou liečbou medzi 12 mačkami so vzorkami výpotkov dostupnými na testovanie ( Obrázok 7). Absencia rýchleho poklesu hladín vírusovej RNA u mačky CT16 spolu s ťažkou lymfopéniou môže vysvetľovať, prečo nereagovala na liečbu. CT10 tiež mala o niečo pomalší pokles hladiny vírusu a po antivírusovej liečbe dvakrát relapsovala. Je pozoruhodné, že hladiny vírusovej RNA v bunkách ascitu u mačiek CT15, CT17 a CT18 klesali najrýchlejšie a boli tiež medzi piatimi mačkami, u ktorých došlo k trvalej remisii ochorenia. Či príčinou bola vlastnosť jednotlivých izolátov FIPV, alebo forma a závažnosť choroby hostiteľa nebolo zistené.

Relatívne počiatočné hladiny RNA vírusu infekčnej peritonitídy mačiek (FIPV) vo výpotkových vzorkách pacientov pred antivírusovou liečbou. Na vzorkách efúzií pacientov pred zahájením liečby sa uskutočnila kvantitatívna PCR v reálnom čase. Relatívne základné hladiny vírusovej RNA ako násobné rozdiely v porovnaní s úrovňou vírusu pred liečbou CT02, mačka s najnižšími hladinami RNA. Úroveň transkriptov RNA bola vypočítaná pre každého pacienta pomocou metódy ∆Ct s referenčným génom pre beta-aktín

Zníženie RNA vírusu mačacej infekčnej peritonitídy zo sekvenčných vzoriek výpotku počas liečby GC376 u mačiek CT10, CT12, CT15, CT16, CT17, CT18 a CT23. Každý bod označuje násobné zníženie hladiny vírusovej RNA oproti hladine nameranej pred liečbou (deň 0). Hladiny vírusovej RNA sa stanovili pomocou kvantitatívnej PCR v reálnom čase metódou ∆Ct a beta-aktín referenčným génom
Zlyhanie liečby v dôsledku recidívy brušnej FIP alebo výskytu neurologického ochorenia
Trinásť z 20 mačiek v teste nakoniec podľahlo recidíve choroby. Jedna mačka (CT16) nevykázala významné zlepšenie a bola eutanizovaná 3 týždne po začiatku 4-týždňového liečebného režimu (obrázky 2 a 8), 8), zatiaľ čo u ostatných 12 došlo k variabilnému obdobiu remisie ochorenia po primárnej alebo sekundárnej liečbe trvajúcej 3–17 týždňov (priemerne 7,8 týždňa) (obrázok 2). Všetky z týchto 13 mačiek okrem jednej (CT09) boli pitvané (tabuľka 1). Osem z týchto mačiek bolo eutanizovaných kvôli závažným neurologickým príznakom a päť z dôvodu recidívy brušnej choroby (obrázok 2). Pri vyšetrení boli sekundárne detekované tri mačky, ktoré podľahli neurologickému ochoreniu (CT05, CT08, CT13) v dôsledku okulárnej FIP (tabuľka 1). Medzi najskoršie príznaky neurologického ochorenia patrili horúčka, ktorá pretrvávala aj napriek pokračujúcej liečbe, apatia, občasné svalové zášklby uší a svalov, neobvyklé pohyby pri prehĺtaní, nutkavé naťahovanie končatín a strata normálnej mentality, ktorá sa prejavila krátkymi epizódami strnulých pohľadov alebo chradnutím. Tieto príznaky pretrvávali pri liečbe niekoľko dní alebo týždňov, ale nakoniec došlo k nekoordinácii a tonickým/klonickým záchvatom. Výskyt a rýchla progresia neurologických príznakov po prerušení liečby boli výraznejšie, ako počas liečby (obrázok 2).
Päť mačiek (CT03, CT07, CT10, CT14 a CT16) malo recidívu typických intraabdominálnych lézií pri absencii neurologických príznakov počas alebo po liečbe (tabuľka 1). U štyroch z nich sa vyskytli ileocekálne útvary (CT03, CT07 a CT14) alebo zväčšená lymfatická uzlina hrubého čreva (CT10), ktorá sa po primárnej liečbe zmenšila (CT03, CT10 a CT14) alebo už nebola hmatateľná (CT07). Avšak CT03 naďalej trpela ťažkou zápchou, napínaním a stolicou podobajúcou sa zubnej paste. Závažnosť obštrukcie hrubého čreva si vyžiadala resekciu hrubého čreva, ktorá zmiernila klinické príznaky, ale nezabránila prípadnému opätovnému výskytu brušných choroby. Všetky tri mačky, u ktorých sa vyskytli silné ileo-cekálno-kolické infiltráty, stále vykazovali dôkazy o tejto forme FIP pri pitve a imunohistochémia preukázala antigén FIPV v makrofágoch v granulomatóznom zápale (obrázok 9).

Rez zo silne zhrubnutej steny resekovaného hrubého čreva z mačky CT03. Imunoperoxidáza (hnedá farba) sfarbená na mačací antigén vírusu infekčnej peritonitídy je pozorovaná v makrofágoch okolo periférie granulomatóznej lézie. K perzistencii vírusu v hrubom čreve došlo počas liečby a ústupu ďalších príznakov ochorenia (napr. efuzívnej peritonitídy)
Pokusy o liečbu neurologickej choroby zvýšením dávky lieku a predĺžením trvania liečby
Pre zmiernenie neurologických príznakov sme sa pokúsili zvýšiť dávku GC376, čím sa zvýšila jeho hladina v krvi a množstvo liečiva, ktoré prešlo cez hematoencefalickú bariéru. Mačka CT01 vykazovala efúznu FIP a bola pôvodne liečená GC376 (10 mg/kg q12h SC po dobu 9 dní). Mačka reagovala dobre, ale v 9. deň sa horúčka sa vrátila a dávka sa zvýšila na 15mg/kg každých 12 hodín po dobu 5 dní. Horúčka zmizla a liečba bola ukončená v deň 14. O 3 dni neskôr sa horúčka vrátila spolu s neurčitými neurologickými príznakmi pozostávajúcimi zo zášklbu svalov, abnormálneho naťahovania končatín a abnormálnych hltacích pohybov. Mačke bola okamžite znovu nasadená dávka 15 mg/kg každých 12h SC a jej stav sa zlepšil, ale krátko potom sa zhoršil s návratom horúčky a rovnakými neurčitými neurologickými príznakmi s miernou nekoordináciou. Dávka sa potom zvýšila na 50 mg/kg každých 12 hodín SC po dobu 14 dní a jej stav sa zlepšil na takmer normálny stav. Liečba bola zastavená, ale okamžite sa vrátili neurologické príznaky. Mačka bola potom liečená ďalšie štyri dni dávkou 50 mg/kg q12 h SC, počas ktorých sa neurologické príznaky opäť zlepšili. Padlo však rozhodnutie ukončiť liečbu úplne. Stav mačky zostal stabilný 1 týždeň a potom sa u nej rozvinula extrémna nekoordinácia, demencia a tonické/klonické záchvaty. Bola vykonaná eutanázia a pitva preukázala lézie iba v mozgu.
Mačka CT12 dobre reagovala na liečbu dávkou 15 mg/kg q12 h SC; rektálna teplota sa vrátila k normálu do 48 hodín a brušný výpotok zmizol do 2 týždňov. Mačka sa po druhom týždni liečby javila ako normálna, potom však mala pretrvávajúcu horúčku 38,9–40°C. Majitelia cítili, že mačka má inak normálnu aktivitu a chuť k jedlu, takže liečba pokračovala v rovnakom dávkovaní. Horúčka však pretrvávala, boli zaznamenané jemné príznaky zmeny správania a mačka nerástla podľa očakávania. Mačka pokračovala v liečbe ďalších 15 týždňov, počas ktorých sa dávka liečiva prechodne dvakrát znižovala (tj. na 10 mg/kg každých 12 hodín a 15 mg/kg každých 24 hodín) počas niekoľkých dní, horúčka sa však zvýšila a zakaždým sa znížila aktivita. Obnovilo sa dávkovanie 15mg/kg každých 12 hodín. Mačka naďalej vykazovala príznaky premenlivej horúčky a nejasné príznaky správania, ale majitelia boli optimistickí, pokiaľ ide o apetít a úroveň aktivity mačky. Liečba mačky bola potom zastavená, pretože ďalšie použitie lieku na tento účel nebolo možné odôvodniť. Stav mačky zostal nezmenený s pretrvávajúcou horúčkou, samotárskym správaním a zastavením rastu ďalších 5 týždňov. V 22. týždni sa objavili závažné neurologické príznaky pozostávajúce z nekoordinácie, demencie a záchvatov a mačka bola eutanizovaná. Makroskopické i mikroskopické lézie boli obmedzené na mozog.
Testovanie na vznik vírusovej rezistencie
O vzniku vírusu rezistentného na liečivo sa uvažovalo u mačky CT03, u ktorej došlo k relapsu s brušnými léziami po počiatočnej priaznivej reakcii na liečbu granulomatóznej kolitídy a zmiešanej FIP. V čase pitvy boli v brušnej dutine stále prítomné granulomatózne lézie a v mozgu sa nenašli žiadne makroskopické ani mikroskopické lézie (tabuľka 1). Preto recidíva ochorenia nesúvisela s neurologickým ochorením a perzistentný antigén FIPV bol identifikovaný v makrofágoch v granulomatóznych léziách. Uskutočnilo sa sekvenčné porovnanie medzi 3CLpro z efúzie pred liečbou a z omenta odobratým pri pitve o 95 dní neskôr. V 3CLpro sa však nenašla žiadna substitúcia aminokyselín, čo naznačuje, že výskyt vírusu rezistentného na liečivá nebol príčinou opakovaného ochorenia mačky.
Porovnávali sa tiež 3CLpro sekvencie vírusovej RNA pred liečbou s tými, ktoré boli získané o 25 dní (CT16), 139 dní (CT02), 149 dní (CT12) a 231 dní (CT10) neskôr v čase pitvy. V tomto období neboli pozorované žiadne rozdiely v 3CLpro. Sekvencie tiež zostali nezmenené u CT02, CT16 a CT12 od času prijatia až po pitvu. Vírusová 3CLpro z pľúc a sleziny mačky CT10, ktorá relapsovala dvakrát počas 8 mesiacov a bola znovu liečená, vykazovala substitúciu Asp-to-Ser v polohe 25 a substitúciu Lys-to-Asp v polohe 260 v porovnaní s vírusom z abdominálnej kvapaliny získanej pred liečbou. Presné účinky týchto mutácií na funkciu proteázy sa v súčasnosti skúmajú. Uvádza sa, že genetická evolúcia kvázi druhov vírusových proteínov nastáva v priebehu času u pacientov chronicky infikovaných RNA vírusom (HCV) a môže viesť k sporadickým zmenám aminokyselín.
Výskyt trvalých klinických remisií
Sedem z 20 mačiek v štúdii liečby GC376, z ktorých všetky absolvovali najmenej 12 týždňov nepretržitej liečby, bolo kategorizovaných ako potenciálne liečebné úspechy na základe viac ako 12 týždňov trvajúcej remisie choroby po ukončení liečby (Obrázok 2). Šesť z týchto mačiatok malo vo veku 3,3–4,4 mesiaca akútnu efúznu brušnú (CT15, CT17, CT18, CT21, CT23) alebo pleurálnu (CT20) formu ochorenia a boli liečené nepretržite 12 alebo 17 (mačka CT21) týždňov (tabuľka 1, obrázok 2). Siedma mačka (CT04), 6,8-ročný krížený kastrovaný kocúr so suchou FIP obmedzenou na mezenterickú lymfatickú uzlinu, tiež dosiahol dlhodobú remisiu, ale až po štyroch cykloch liečby so zvyšujúcim sa trvaním (Tabuľka 1, Obrázok 2).
Šesť z týchto dlhodobo preživších mačiek malo na začiatku liečby abnormality v CBC, hematokrite a celkových proteínoch, ale v čase ukončenia liečby mali úplne normálne hodnoty v krvi. Avšak mačka CT21 mala aj po 12 týždňoch zvýšené hladiny bielkovín v plazme a zvýšený počet bielych krviniek a v liečbe pokračovala ďalších 5 týždňov. Počty plazmatických bielkovín a bielych krviniek sa zlepšili po ďalších 5 týždňoch liečby, stále však neboli v referenčnom rozsahu. Trinásť týždňov po ukončení liečby sa u mačky vyvinul typický FIP výpotok v hrudnej dutine s horúčkou. Tekutina z hrudníka bola odsatá, aby sa zlepšilo dýchanie, a mačka začala s druhým kolom GC376 a v čase písania článku bola afebrilná, aktívna a po 8 týždňoch liečby jedla normálne. Liečba bude trvať 12 týždňov, ak sa znova neobjavia žiadne známky ochorenia.
Vedľajšie účinky pozorované počas liečby a po liečbe
Počas a po liečbe GC376 boli pozorované dva vedľajšie účinky. Liek pri injekčnej aplikácii často spôsoboval štípanie/pálenie. Subkutánne opuchy sa vyskytli, keď sa v rovnakom mieste aplikovalo príliš veľa injekcií, ale tie rýchlo ustúpili. U jednej mačky (CT12) sa približne v 14. týždni 18-týždňového obdobia liečby vyskytla hlboko lokalizovaná ulcerácia medzi lopatkami. Pri pitve však nebol pozorovaný žiadny dôkaz dermálnej FIP a išlo pravdepodobne o reakciu na nepretržité injekcie v rovnakom mieste. Prieskum siedmich dlhodobo preživších mačiek preukázal citeľné ohniskové podkožné zhrubnutie. U jednej mačky sa na röntgenových snímkach objavili štyri zvápenatené hrčky veľkosti hrášku. Tieto hrčky boli chirurgicky odstránené spolu s okolitým fibrotickým tkanivom. Traja ďalší dlhodobo preživší majú 1–3 malé ohniskové oblasti s trvalou stratou chlpov v miestach vpichu, ktoré sú zakryté okolitým srsťou (obrázok 10). Majitelia a ich veterinári boli požiadaní, aby tieto lézie pravidelne kontrolovali kvôli prípadným zmenám, či výskytu nových lézií.

Ohnisková oblasť permanentného vypadávania chlpov spôsobená nechceným ukladaním GC376 do epidermy mačky CT21. Tieto oblasti boli zvyčajne prekryté chlpmi a neboli zvonka viditeľné
Najvýznamnejším vedľajším účinkom spojeným s dlhodobou liečbou bol juvenilný chrup. Normálna tvorba, rast a prerezanie trvalých zubov sa oneskorili u všetkých štyroch liečených mačiatok vo veku 3,3–4,4 mesiaca. Očné zuby, rezáky, štvrtý premolár a molár boli postihnuté najmenej, zatiaľ čo druhý a tretí premolár boli postihnuté najviac (obrázok 11). Dospelé zuby sa javili menšie ako normlingválne a to spolu s oneskoreným prerezaním viedlo buď k ponechaniu mliečnych špičákov, nevypadnutiu mliečnych zubov alebo k čiastočnému prerezaniu abnormálnych trvalých zubov k súčasne ponechaným mliečnym zubom. U žiadneho z dlhodobo preživších neboli pozorované žiadne iné anatomické alebo fyziologické defekty a neboli zaznamenané ani u pitvaných mačiek.
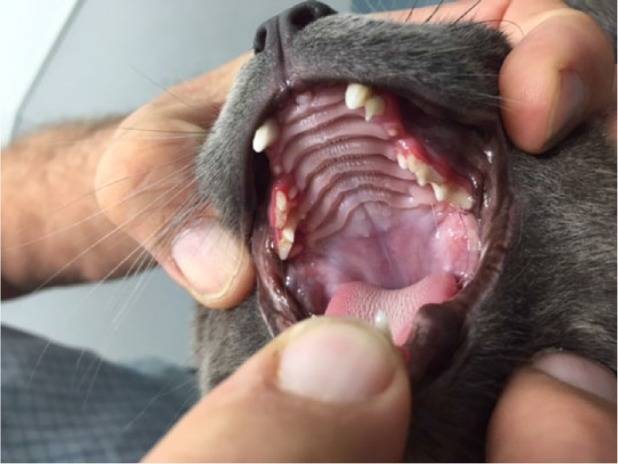
Dospelý chrup mačky CT17, ktorá bola liečená 12 týždňov GC376, počnúc vekom 4,4 mesiaca. Je viditeľný ponechaný horný ľavý mliečny špičák. Zdá sa, že horný druhý a tretí premolár sú mliečne. Malé trvalé tretie premoláre sa čiastočne prerezali lingválne k mliečnym tretím horným premolárom. Gingiva obklopujúca ponechaný špičák a premoláre je zapálená. Dospelé špičáky sa javia tiež menšie ako zvyčajne. Zdá sa, že trvalý pravý špičák a štvrtý horný premolár sa prerezali normálne
Pitevné nálezy
Telá 12/13 mačiek, u ktorých liečba nebola úspešná, boli podrobené pitve vrátane hrubého a histologického vyšetrenia a imunohistochémie postihnutých tkanív pre FIPV antigén. Odobrané a vyšetrené tkanivá zahŕňali reprezentatívne rezy všetkých hlavných brušných a hrudných orgánov, mozgu a očí. Hrubé vyšetrenie identifikovalo tri odlišné prezentácie. Päť mačiek nejavilo výrazné známky aktívnej FIP (CT01, CT02, CT05, CT08, C12), tri mali lézie zodpovedajúce neefúznej FIP (CT07, CT10, CT13) a štyri mali efúznu peritonitídu s multiorgánovým postihnutím (CT03, CT14, CT16, CT22). Histológia piatich mačiek, ktoré nevykazovali dostatočné dôkazy o chorobe, preukázala väčšinou mierne mononukleárne infiltráty, zvyčajne perivaskulárny zápal v oku, pečeni, črevnej stene a obličkách. Tri mačky s neefúznou FIP mali mierny až závažný zápal v mnohých orgánoch s najťažšími léziami v oku, mezenterických lymfatických uzlinách, obličkách a pľúcach. Tri mačky s efúznou FIP mali závažný pyogranulomatózny zápal vo viacerých brušných orgánoch vrátane omenta, pobrušnice, črevnej steny, mezenterických lymfatických uzlín, pečene a sleziny.
Závažný zápal typický pre cerebrálnu FIP bol prítomný v mozgu všetkých okrem jednej (CT07) z ôsmich mačiek, ktoré sa podrobili pitve bez výrazných hrubých známok FIP alebo s neefúznou FIP. Jedna mačka bez charakteristických mozgových lézií mala ťažký mozgový edém. Naproti tomu typické FIP lézie chýbali v mozgu všetkých troch pitvaných mačiek s efúznou FIP. Stereotypné FIP lézie mozgu boli charakterizované stredne ťažkou až ťažkou chronickou meningoencefalitídou a ventrikulitídou spojenou s periventrikulárnou nekrózou parenchýmu (obrázok 12a). Štvrtá komora bola postihnutá najťažšie a meningitída bola najčastejšie pozorovaná ventrálne do malého mozgu a mozgového kmeňa. Často sa pozorovali silné perivaskulárne manžety spojené s vaskulitídou. FIP antigén sa demonštroval imunoperoxidázovým zafarbením v mozgu 6/7 prípadov stereotypnej cerebrálnej FIP (obrázok 12b). Tkanivá z 11 pitvaných mačiek, sa testovali na prítomnosť FIPV RNA pomocou qRT-PCR. Všetky vykázali pozitívny výsledok, čím sa stanovila perzistencia vírusu u mačiek, u ktorých liečba nebola úspešná.

Fotomikrografy lézie v mozgu mačky CT08. U tejto mačky sa počas počiatočnej liečby GC376 vyskytlo závažné neurologické ochorenie. (a) Štvrtá komora obsahuje bielkovinovú tekutinu zmiešanú s početnými neutrofilmi a makrofágmi, ktoré multifokálne zasahujú do okolitého zriedeného neuropilu. Veľké manžety lymfocytov a plazmatických buniek obklopujú krvné cievy (*) (farbenie hematoxylínom, zväčšenie 20x). (b) Viaceré bunky pripomínajúce peritoneálne makrofágy (vyznačená malá oblasť na obrázku 12a) vykazujú pozitívnu imunoreaktivitu pre mačací infekčný antigén peritonitídy (kontrastné farbivo hematoxylín, zväčšenie 600x).
Diskusia
Úspech v liečbe GC376 pri experimentálnej infekcii FIPV nás motivoval k preskúmaniu účinnosti GC376 pri prirodzene vyvinutej FIP. Medzi experimentálnou efúznou brušnou FIP a prirodzene sa vyskytujúcou chorobou existujú významné rozdiely. Experimentálna choroba obchádza kritické počiatočné štádium, ktoré začína u mačiatok vystavením neškodnému mačaciemu enterickému koronavírusu (FECV). Prirodzene sa vyskytujúca FIP je výsledkom špecifických mutantov, ktoré vznikajú po infekcii FECV, a FIP sa vyskytuje za prítomnosti imunity voči FECV. Experimentálna FIP je naopak indukovaná u mačiek, ktoré sa nestretli s koronavírusom intraperitoneálnou injekciou veľkej dávky purifikovaného FIPV získaného od laboratórnej mačky. Prirodzene sa vyskytujúca choroba je často subklinická po mnoho týždňov alebo mesiacov pred pozorovaním vonkajších príznakov choroby, zatiaľ čo experimentálne príznaky choroby sa objavia do 2–4 týždňov a rýchlo progredujú. Prirodzene sa vyskytujúca FIP má rôzne klinické formy, zatiaľ čo experimentálna infekcia má takmer vždy abdominálnu efúznu podobu. FIP v prírode je tiež ovplyvnená prostredím chorobu zvyšujúcich kofaktorov, zatiaľ čo experimentálne ochorenie sa vyskytuje u mačiek bez vonkajších vplyvov. Rozdiely môžu vysvetľovať, prečo sa choroba vyvinie len u malej časti mačiek prirodzene vystavených FIPV, zatiaľ čo 80–100% experimentálne infikovaných mačiek zomiera. Naše predpovede sa ukázali ako správne a prirodzene sa vyskytujúca FIP sa liečila oveľa ťažšie ako experimentálna choroba. Je však potrebné zdôrazniť, že tento pokus by nebol schválený bez informácií získaných z farmakokinetických štúdií, štúdií akútnej a chronickej toxicity a účinnosti uskutočňovaných na laboratórnych mačkách.
Bol to prvý pokus o použitie cieleného antivírusového lieku proti systémovému a vysoko smrteľnému veterinárne významnému ochoreniu. Aj keď zatiaľ nie sú k dispozícii žiadne špecifické antivírusové lieky na koronavírusové infekcie u ľudí alebo zvierat, na liečbu boli vyvinuté antivírusové lieky na iné vírusové infekcie ľudí, ako sú HCV a HIV-1, a použitie týchto liekov poskytlo solídny základ pre ich aplikáciu na choroby zvierat, ako je FIP. HCV infikuje hlavne pečeňové bunky a u väčšiny ľudí spôsobuje pretrvávajúcu vírusovú infekciu. Avšak len asi u 20–30% z nich sa rozvinú ochorenia pečene v časovom horizonte 20–30 rokov. Infekciu HCV je možné eliminovať nešpecifickou antivírusovou liečbou (interferón a ribavirín) po dobu 6–12 mesiacov u približne polovice pacientov a nedávnym zavedením priamo pôsobiacich antivírusových liekov v trvaní 3–6 mesiacov sa počas liečby podstatne zvýšila miera vyliečenia na viac ako 90% . HIV infekcia u ľudí vedie k predĺženému asymptomatickému stavu a nakoniec k pokročilému ochoreniu na HIV. HIV-1 infikuje T lymfocyty a makrofágy a prežíva v latentnom stave. Viac ako 30 antiretrovírusových liekov, z ktorých väčšina sa používa v kombinácii dvoch alebo viacerých liekov, sa úspešne použilo na zníženie vírusovej záťaže na nedetegovateľnú hladinu v krvi pacientov s HIV/AIDS. Vírus sa však po prerušení antivírusovej liečby vracia a vyžaduje tak celoživotnú antivírusovú liečbu. Šírenie vírusu do mozgu, ktoré je sprostredkované hlavne vírusom infikovanými makrofágmi, a následný vývoj neurologického ochorenia sa vyskytuje u viac ako 50% infekcií HIV. Neurologické zhoršenie preto stále zostáva dôležitým problémom aj v tejto dobe antivírusovej liečby. Tieto precedensy antivírusovej liečby infekcií HCV a HIV-1 ukazujú, že výsledok liečby (vírusový klírens vs perzistencia vírusu), trvanie liečby (konečná vs kontinuálna) a prítomnosť neurologických následkov sú výrazne ovplyvnené vírusovou patogenézou.
Táto štúdia bola obmedzená na 20 mačiek s FIP, ktoré predstavovali spektrum veku a foriem choroby. Aj keď bol počet liečených mačiek malý, zhromaždilo sa prekvapivé množstvo informácií, napríklad o tom, ako dlho sa má liečiť, o možných vedľajších účinkoch, o tom, ako identifikovať klinickú formu FIP, ktorá bude s najväčšou pravdepodobnosťou reagovať na liečbu, a potenciálnych ukazovateľoch zlyhania liečby a jej úspešnosti. Klinická štúdia bola založená na skúsenostiach získaných z farmakokinetických štúdií a štúdií účinnosti vykonaných na laboratórnych mačkách. Počiatočné obdobie liečby bolo na základe experimentálnych štúdií stanovené na 2 týždne, nakoniec sa však predĺžilo na 12 týždňov a viac na základe skúseností získaných v priebehu testovania. Toto konečné liečebné obdobie sa blížilo k 3–6 mesiacom používaným na liečbu infekcie HCV u ľudí s priamo pôsobiacimi antivírusovými liekmi. Na základe experimentálnych štúdií boli očakávané ťažkosti s liečením neurologických foriem choroby. Vedľajšie účinky boli prijateľné a zahŕňali pálenie pri aplikácii injekcie a dermálny a podkožný zápal, keď sa na rovnaké miesta podalo príliš veľa liečiva. Tento jav bol už predtým pozorovaný aj u laboratórnych mačiek. Závažnejší vedľajší účinok, ktorý sa predtým u laboratórnych mačiek nepozoroval, sa obmedzil na mačiatka a zahŕňal spomalený vývoj dospelých zubov a retenciu alebo oneskorenú stratu mliečnych zubov.
Liečba GC376 bola úspešná v indukcii významnej remisie príznakov ochorenia a regresie lézií u 19/20 mačiek. Tento výsledok potvrdzuje naše zistenia rýchleho zvratu klinických príznakov u laboratórnych mačiek s experimentálnou FIP liečených GC376, a rozšíril naše znalosti o účinkoch lieku na široké spektrum foriem prirodzene sa vyskytujúcej FIP. Mačky pochádzali z rôznych častí USA a dokonca aj z Peru, čo potvrdzuje, že geograficky rozmanité kmene FIPV boli voči tomuto inhibítoru rovnako citlivé. K výraznému zníženiu transkriptov vírusovej RNA vo výpotkoch došlo v priebehu niekoľkých dní liečby spolu s rýchlym zlepšením zdravotného stavu. Remisia ochorenia však pretrvávala 3 mesiace a dlhšie iba u 7/20 týchto mačiek. Neschopnosť dosiahnuť dlhodobú remisiu ochorenia bola nakoniec spojená s výskytom neurologického ochorenia pri absencii rozsiahlych brušných lézií alebo s opakovaním/pretrvávaním rozsiahlych brušných lézií za prítomnosti histologických lézií v mozgu a/alebo v očiach. Tieto objavy naznačujú, že FIPV má väčšiu tendenciu šíriť sa z telesných dutín do mozgu, ako sa pôvodne predpokladalo, najmä ak sa mu poskytne dostatok času. Toto rozšírenie s najväčšou pravdepodobnosťou zahŕňa infikované makrofágy, ktoré vstupujú do mozgu malými krvnými cievami v mozgových blanách a ependyme.
U mačky, u ktorých sa vyskytlo neurologické ochorenie, sa tak stalo buď počas liečby (CT05, CT08, CT22), alebo 2 (CT01, CT02, CT09), 3 (CT13) alebo 6 (CT10) týždňov po ukončení liečby. Najpravdepodobnejším vysvetlením tohto oneskorenia, ako aj určitej terapeutickej výhody vyšších dávok, bolo to, že časť GC376 bola stále schopná preniknúť do mozgu. Hladiny GC376 v mozgovomiechovom moku predstavovali iba 3% plazmy v mozgu 2 hodiny po subkutánnej injekcii v dávke 10 mg/kg (nezverejnené údaje). Aj keď boli relatívne koncentrácie liečiva v mozgu u týchto mačiek nízke, stále boli 21,4-krát vyššie ako hladiny potrebné na inhibíciu replikácie vírusu v tkanivovej kultúre. Na základe tohto zistenia sa predpokladalo, že vyššie dávky umožňujú prienik vyššieho množstva liečiva do mozgu. Tento predpoklad bol podporený skúsenosťami s dvoma mačkami, ktoré vykazovali neurologické príznaky. Zvýšenie dávky GC376 na 50 mg/kg každých 12 hodín u jednej mačky (CT01) viedlo k znateľnému zlepšeniu, ale neeliminovalo príznaky ochorenia mozgu. Zdá sa, že predĺženie liečby o takmer 3 mesiace v dávke 15mg/kg každých 12 h oddialilo progresiu neurologických príznakov u druhej mačky (CT12), zatiaľ čo pokusy znížiť celkovú dennú dávku u tejto mačky na 10mg/kg každých 12 hodín alebo 15mg/kg každých 24 hodín spôsobili zhoršenie neurologických príznakov. To naznačuje, že dávky 15 mg/kg každých 12 hodín alebo vyššie umožnili dostatočnému množstvu GC376 prekonať hematoencefalickú bariéru, aby spomalil, ale neeliminoval neurologické príznaky.
Vysoký výskyt ochorení centrálneho nervového systému (CNS) v tejto štúdii bol vyšší, ako sa uvádzalo predtým, a bol neočakávaný, pretože mačky so známkami postihnutia mozgu alebo miechy boli zo štúdie vylúčené. Choroby CNS sa ukázala omnoho pravdepodobnejšia u starších mačiek so suchou alebo zmiešanou formou FIP ako u mladých mačiek s vlhkou FIP. To naznačuje, že FIPV môže u mnohých mačiek preniknúť do mozgu, ak je mu poskytnutý dostatok času. Zdá sa, že pri infekcii CNS zohrávajú úlohu makrofágy peritoneálneho typu, pretože FIPV infikované bunky v mozgu mačiek s neurologickou FIP sa viac podobajú skôr peritoneálnym makrofágom ako rezidentným mozgovým makrofágom. To by nemalo byť prekvapujúce, pretože makrofágy migrujú do rôznych tkanív, vrátane mozgu, na vykonávanie imunitného dohľadu a sú tiež cieľmi pre celý rad infekčných agensov, ako sú FIPV a HIV-1. Infikované makrofágy hrajú hlavnú úlohu pri šírení vírusu do mozgu u pacientov s HIV a detekcia vírusu v mozgu je možná v priebehu niekoľkých týždňov po infikovaní. K neurologickému poškodeniu však zvyčajne dôjde v neskoršom štádiu. Lieky proti HIV tiež znižujú frekvenciu závažných neurologických porúch, podobne, ako sa pozorovalo v tejto štúdii o FIPV a GC376. Existujú aj alternatívne vysvetlenia. Je možné, že extra-CNS účasť môže inhibovať rozvoj mozgových ochorení a naopak. Je bežné, že sa ochorenie CNS vyskytuje pri neprítomnosti viscerálneho ochorenia a naopak. Potlačenie replikácie vírusu v neneuronálnych tkanivách môže tiež zvýšiť pozitívnu selekciu mutantov, ktoré sú neurotropnejšie alebo neurovirulentnejšie. Dôkaz druhej možnosti by si však vyžadoval veľké štúdie s použitím laboratórnych mačiek.
Zdalo sa, že určité formy FIP ovplyvňovali úspešnosť liečby. Chovanie GC376 pri liečbe okulárnej FIP bolo paradoxné, pretože táto forma mimoriadne dobre reagovala na GC376. Aj keď očné lézie reagovali na liečbu, všetky tri mačky s postihnutím očí nakoniec podľahli mozgovým ochoreniam, čo podporilo blízky anatomický vzťah oka a CNS. Chronické ileocekálne postihnutie a postihnutie hrubého čreva a spomalený rast u starších mačiek v tejto štúdii taktiež predstavovali zlú prognózu. U mnohých z týchto mačiek sa objavil brušný výpotok iba ako terminálny prejav ich choroby. Hostiteľské faktory tiež spojené so zníženou odpoveďou na antivírusovú liečbu pri iných vírusových infekciách, ako je HCV, zahŕňajú vek, pohlavie, cirhózu alebo fibrózu pečene, rasu alebo telesnú hmotnosť.
Vznik rezistencie je hlavným problémom každého antivírusového lieku, ale FIPV sa zriedka prenáša z mačky na mačku, a rezistencia na liečivo, ak by sa vyskytla, by predstavovala problém iba pre jednotlivé liečené mačky, a nie pre celú populáciu. Aj keď vírusová rezistencia na GC376 nebola pozorovaná až do 20 pasáží in vitro, čo naznačuje, že rezistencia sa nedá získať ľahko, dlhodobá a opakovaná liečba in vivo môže predstavovať silnejší selekčný faktor. Zdá sa však, že vírusová rezistencia nebola zodpovedná za relapsy brušných chorôb u piatich liečených mačiek. Tieto mačky mali granulomatózne útvary, často v hrubom čreve a ileo-cekálno-kolických lymfatických uzlinách, ktoré mohli poskytovať chránené miesto na pretrvanie vírusov. Ochrana patogénov v granulómoch je pre mykobaktérie dobre zdokumentovaným javom a vzťahuje sa na ďalšie patogény, ako sú vírusy. Stav ochorenia pečene (cirhóza) pri infekcii HCV tiež zvyšuje riziko relapsu a vyžaduje dlhšiu liečbu, čo tiež naznačuje, že vírusy môžu byť chránené pred liekmi, keď sa nachádzajú na určitých chránených miestach. Formácia „ochranných granulómov“ zahŕňa veľké množstvo chemokínov a cytokínov a zvyšovanie regulácie chemokínových receptorov, adresínov, selektínov a integrínov. Perzistencia patogénov na týchto chránených miestach môže vyžadovať vyššiu dávka lieku a dlhšiu dobu trvania liečby.
Zlyhania liečby môžu tiež byť výsledkom neschopnosti hostiteľa dosiahnuť ochrannú imunitnú reakciu počas obdobia, keď je potlačená replikácia vírusu. Takéto zlyhanie sa pozorovalo pri infekcii HCV u ľudí. Imunita sprostredkovaná T-lymfocytmi hrá dôležitú úlohu v ochrannej imunite, ktorá sa vyskytuje asi u 20% akútnej infekcie HCV, a pri rovnakom alebo väčšom podiele infekcie FIPV. Je ešte potrebné preskúmať možnú synergiu vírusového klírensu sprostredkovaného T-lymfocytmi a antivírusovej terapie u mačiek s FIP. Prínosom by mohla byť aj kombinácia antivírusových liekov a stimulantov imunity T-lymfocytov pri liečbe FIP, ako je kombinácia interferónov a ribavirínu pri liečbe infekcie HCV.
Trvalá remisia u 6/7 mačiek liečených 12 týždňov alebo dlhšie bola do istej miery predvídateľná. Tieto mačky boli vo veku 3,3–4,4 mesiaca, keď sa u nich prejavili akútne príznaky brušnej (C15, C17, C18, CT21, CT23) alebo hrudnej efúznej FIP (CT20). To ich urobilo mladšími ako všetky ostatné mačky v štúdii okrem troch (CT8, CT16, CT21) a viac sa podobali 16-týždňovým laboratórnym mačkám s akútnym nástupom efúznej FIP, ktoré dobre reagovali na GC376. Choroba, ak je akútna, dáva vírusu na prienik do mozgu alebo očí málo času. Akútnosť ich ochorenia mohla tiež umožniť kratšiu dobu, aby infekcia natrvalo narušila akúkoľvek ochrannú imunitnú odpoveď. Siedma mačka, CT04, bola oproti týmto šiestim mladším mačkám extrémom. CT04 bola so svojimi 6,8 rokmi najstaršou mačkou v štúdii, u ktorej došlo k výraznému úbytku hmotnosti (30%) a ochoreniu obmedzenému na mezenterické lymfatické uzliny. CT04 utrpela relapsy choroby vyžadujúce obnovenie liečby, ale všetky relapsy boli identické so vstupým stavom a nezahŕňali CNS. Je známe, že mačky s touto formou FIP prechádzajú spontánnou remisiou, čo naznačuje, že existuje bod zlomu medzi imunitou a chorobou. Mačky CT04 a CT21 demonštrovali múdre rozhodnutie znovuzahájenia liečby pri relapse, za predpokladu, že relapsy nezahŕňajú oči alebo nervový systém a stále reagujú na lieky.
Stanovenie minimálnej doby trvania liečby bolo založené na postupnom predlžovaní trvania liečby na základe priaznivej reakcie na liečbu. Na základe experimentálnych štúdií sa očakávalo, že môžu byť postačujúce 2 týždne liečby; to sa teda použilo ako východiskový bod. Táto štúdia však naznačila, že minimálna doba liečby sa blížila k 12 týždňom, čo sa prekvapivo blížilo k zvyčajnému 12-týždňovému obdobiu, ktoré je potrebné na liečbu ľudí s HCV pomocou inhibítorov proteázy. Avšak doba liečby HCV sa môže pohybovať od 8 do 24 týždňov u rôznych ľudí. Mačka CT21 bola navonok zdravá, aktívna a po 12 týždňoch liečby rástla, ale celkový počet bielkovín a bielych krviniek sa stále nevrátil do normálu, ako tomu bolo u ostatných šiestich mačiek. Napriek tomu sa rozhodlo o ukončení liečby po 17 týždňoch z dôvodu dlhého obdobia navonok normálneho zdravia. To, či by dlhodobejšia liečba mohla zabrániť relapsu choroby 13 týždňov po ukončení liečby, si môžeme len domýšľať, ale zvyšuje to pochybnosť o tom, aká dlhá má vôbec byť potrebná doba liečby u niektorých mačiek. Nastoľuje sa tiež otázka, ako dlhé musí byť obdobie remisie, aby sme mohli prehlásiť že došlo k uzdraveniu, a nielen k dlhodobej remisii. Najdlhšie obdobie bez choroby bolo v čase písania tohto článku viac ako 11 mesiacov, pričom päť ďalších mačiek bolo bez známok infekcie po dobu 5–9 mesiacov. Na základe klinických a histologických dôkazov neurologického ochorenia v čase smrteľných relapsov sa zdá, že sa vírus nakoniec dostane do mozgu a že to môže byť najdôležitejším obmedzujúcim faktorom pri antivírusovej liečbe FIP.
Aj keď dlhodobo prežila iba jedna tretina mačiek, 20 mačiek v tejto štúdii poskytuje základ pre budúce štúdie s GC376 a ďalšími antivírusovými liekmi, ktoré budú nasledovať. Nie všetky mačky budú liečiteľné, ale to by nemalo zastaviť úsilie. V tejto obmedzenej štúdii sa takmer všetkým liečeným mačkám vrátil normálny zdravotný stav, aj keď iba na niekoľko týždňov alebo mesiacov. Je dôležité si uvedomiť univerzálnosť vírusových patogénov a využiť priekopnícky vývoj liekov, ktoré sa klinicky uplatňujú pri liečbe ľudských chorôb, ako je HIV/AIDS, hepatitída C, MERS, SARS, Ebola a chrípka.
Závery
Inhibícia FIPV 3CLpro s pomocou GC376 sa za podmienok štúdie ukázala ako účinná a viedla k zníženiu replikácie vírusu a k remisii príznakov choroby u mačiek s prirodzene sa vyskytujúcou FIP mimo CNS. K trvalej remisii v tejto štúdii však dochádzalo skôr u mačiatok vo veku nižšom ako 18 týždňov s akútnou vlhkou FIP alebo u mačiek so suchou FIP obmedzenou na mezenterickú lymfatickú uzlinu a je menej pravdepodobné, že sa vyskytne u mačiek starších ako 18 týždňov so suchou, zmiešanou alebo okulárnou formou FIP. Neschopnosť dosiahnuť trvalú remisiu bola spojená buď s vysokým výskytom neurologických ochorení počas alebo po ukončení liečby alebo s recidívou brušných lézií. Zdá sa, že antivírusová liečba spomalila progresiu neurologického ochorenia, ale nedokázala ju zvrátiť pri dávke použitej v tejto štúdii. Príčina recidívy extra-neurologického ochorenia pri liečbe nebola stanovená, ale nesúvisela s mutáciami v oblasti viažucej proteázu.
Poznámky pod čiarou
Prijaté: 3.8.2017
Doplňujúci materiál: Formulár informovaného súhlasu majiteľa.
Konflikt záujmov: YK, KOC a WCG majú v rukopise patentové nároky na inhibítory proteázy. Ostatní autori neprehlasujú žiadne potenciálne konflikty záujmov v súvislosti s výskumom, autorstvom alebo publikovaním tohto článku.
Financovanie: Hlavná podpora tejto štúdie bola umožnená vďaka grantu od Morris Animal Foundation, Denver, CO, USA. Ďalšie prostriedky na technickú podporu a starostlivosť o zvieratá poskytli Fond Philipa Raskina, Kansas City, SOCK FIP, grant National Institutes of Health R01AI109039 a Centrum pre zdravie spoločenských zvierat, Kalifornská univerzita, Davis, CA, USA.
Literatúra
| 1. | Prokofjeva, MM, Kochetkov, SN, Prassolov, VS. Therapy of HIV infection: current approaches and prospects. Acta Naturae 2016; 8: 23–32. Google Scholar | Crossref | Medline |
| 2. | Carter, W, Connelly, S, Struble, K. Reinventing HCV treatment: past and future perspectives. J Clin Pharmacol 2017; 57: 287–296. Google Scholar | Crossref | Medline |
| 3. | Kim, Y, Lovell, S, Tiew, KC. Broad-spectrum antivirals against 3C or 3C-like proteases of picornaviruses, noroviruses, and coronaviruses. J Virol 2012; 86: 11754–11762. Google Scholar | Crossref | Medline |
| 4. | Kim, Y, Mandadapu, SR, Groutas, WC. Potent inhibition of feline coronaviruses with peptidyl compounds targeting coronavirus 3C-like protease. Antiviral Res 2013; 97: 161–168. Google Scholar | Crossref | Medline |
| 5. | Kim, Y, Shivanna, V, Narayanan, S. Broad-spectrum inhibitors against 3C-like proteases of feline coronaviruses and feline caliciviruses. J Virol 2015; 89: 4942–4950. Google Scholar | Crossref | Medline |
| 6. | Kim, Y, Liu, H, Galasiti Kankanamalage, AC. Reversal of the progression of fatal coronavirus infection in cats by a broad-spectrum coronavirus protease inhibitor. PLoS Pathog 2016; 12: e1005531. Google Scholar | Crossref | Medline | ISI |
| 7. | Miller, FG, Brody, H. What makes placebo-controlled trials unethical? Am J Bioethics 2002; 2: 3–9. Google Scholar | Crossref | Medline |
| 8. | Chiodo, GT, Tolle, SW, Bevan, L. Placebo-controlled trials good science or medical neglect? West J Med 2000; 172: 271–273. Google Scholar | Crossref | Medline |
| 9. | Van Kruiningen, HJ, Ryan, MJ, Shindel, NM. The classification of feline colitis. J Comp Pathol 1983: 93: 275–294. Google Scholar | Crossref | Medline | ISI |
| 10. | Pedersen, NC, Eckstrand, C, Liu, H. Levels of feline infectious peritonitis virus in blood, effusions, and various tissues and the role of lymphopenia in disease outcome following experimental infection. Vet Microbiol 2015; 175: 157–166. Google Scholar | Crossref | Medline | ISI |
| 11. | Pellerin, M, Lopez-Aquirre, Y, Penin, F. Hepatitis C virus quasispecies variability modulates nonstructural protein 5A transcriptional activation, pointing to cellular compartmentalization of virus-host interactions. J Virol 2004; 78: 4617–4627. Google Scholar | Crossref | Medline |
| 12. | Pedersen, NC, Allen, CE, Lyons, LA. Pathogenesis of feline enteric coronavirus infection. J Feline Med Surg 2008; 10: 529–541. Google Scholar | SAGE Journals | ISI |
| 13. | Pedersen, NC . A review of feline infectious peritonitis virus infection: 1963–2008. J Feline Med Surg 2009; 11: 225–258. Google Scholar |
| 14. | Pedersen, NC . An update on feline infectious peritonitis: virology and immunopathogenesis. Vet J 2014; 201: 123–132. Google Scholar | Crossref | Medline |
| 15. | Pedersen, NC, Liu, H, Durden, M. Natural resistance to experimental feline infectious peritonitis virus infection is decreased rather than increased by positive genetic selection. Vet Immunol Immunopathol 2016; 171: 17–20. Google Scholar | Crossref | Medline | ISI |
| 16. | Pedersen, NC, Liu, H, Gandolfi, B. The influence of age and genetics on natural resistance to experimentally induced feline infectious peritonitis. Vet Immunol Immunopathol 2014; 162: 33–40. Google Scholar | Crossref | Medline |
| 17. | Clifford, DB . HIV-associated neurocognitive disease continues in the antiretroviral era. Top HIV Med 2008; 16: 94–98. Google Scholar | Medline |
| 18. | Foley, JE, Lapointe, JM, Koblik, P. Diagnostic features of clinical neurologic feline infectious peritonitis. J Vet Intern Med 1998; 12: 415–423. Google Scholar | Crossref | Medline | ISI |
| 19. | Mesquita, LP, Hora, AS, de Siqueira, A. Glial response in the central nervous system of cats with feline infectious peritonitis. J Feline Med Surg 2016; 18: 1023–1030. Google Scholar | SAGE Journals | ISI |
| 20. | Pedersen, NC . Feline infectious peritonitis: something old, something new. Feline Pract 1976; 6: 42–51. Google Scholar |
| 21. | Valcour, V, Sithinamsuwan, P, Letendre, S. Pathogenesis of HIV in the central nervous system. Curr HIV/AIDS Rep 2011; 8: 54–61. Google Scholar | Crossref | Medline |
| 22. | Joseph, SB, Arrildt, KT, Sturdevant, CB. HIV-1 target cells in the CNS. J Neurovirol 2015; 21: 276–289. Google Scholar | Crossref | Medline |
| 23. | Spudich, S, Gonzalez-Scarano, F. HIV-1-related central nervous system disase: current issues in pathogenesis, diagnosis and treatment. Cold Spring Harb Perspect Med 2012; 2: a007120 Google Scholar | Crossref | Medline |
| 24. | Cavalcante, LN, Lyra, AC. Predictive factors associated with hepatitis C antiviral therapy response. World J Hepatology 2015; 7: 1617–1631. Google Scholar | Crossref | Medline |
| 25. | Saunders, BM, Cooper, AM. Restraining mycobacteria: role of granulomas in mycobacterial infections. Immunol Cell Biol 2000; 78: 334–334. Google Scholar | Crossref | Medline |
| 26. | Smyk-Pearson, S, Tester, IA, Klarquist, J. Spontaneous recovery in acute human hepatitis C virus infection: functional T-cell thresholds and relative importance of CD4 help. J Virol 2008; 82: 1827–1837. Google Scholar | Crossref | Medline |
| 27. | Legendre, AM, Bartges, JW. Effect of polyprenyl immunostimulant on the survival times of three cats with the dry form of feline infectious peritonitis. J Feline Med Surg 2009; 11: 624–626. Google Scholar | SAGE Journals | ISI |
| 28. | Legendre, AM, Kuritz, T, Galyon, G. Polyprenyl immunostimulant treatment of cats with presumptive non-effusive feline infectious peritonitis in a field study. Front Vet Sci 2017; 4: 7. Google Scholar | Crossref | Medline |


